
硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3 MgO、CaO等,生产工艺流程示意如下:
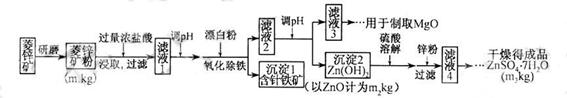
(1) 将菱锌矿研磨成粉的目的是_____。
(2) 完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)2+□____+□_____==□Fe(OH)3 +□CI-
(3)针铁矿(Goethite)是以德国诗人歌德(Go ethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是_______。
ethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是_______。
(4)根据下表数据,调节“滤液 2”的pH时,理论上可选用的最大区间为______。
2”的pH时,理论上可选用的最大区间为______。
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉淀的pH | 10.4 | 6.4 | — | — |
| 沉淀完全的pH | 12.4 | 8.0 | — | — |
| 开始溶解的pH | — | 10.5 | — | — |
| Ksp | 5.6× | — | 6.8× | 2.8× |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是______(选填序号)。
a.大理石粉 b.石灰乳 c. 纯碱溶液 d.烧碱溶液
纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3 的质量分数不低于________。
【解析】(1) 将棱铁矿研磨成粉可以增加反应时的接触面积,使得反应更加充分
(2) 漂白粉的成分中含有次氯酸根,调节酸碱度后,具有较强的氧化性,能使+2价的铁离子氧化成+3价,氧化亚铁变成氧化铁必须增加氢氧元素的量,可以推测出另一种反应物为水,清楚了反应物,一般可以顺利的配平。
(3) 化学式量为89,组成元素是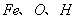 ,其中铁的相对原子量为56,扣掉56剩下33,化学式中只能含有2个氧原子和1个氢原子,所以可能的组成为
,其中铁的相对原子量为56,扣掉56剩下33,化学式中只能含有2个氧原子和1个氢原子,所以可能的组成为
(4)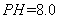
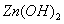 完全沉淀,
完全沉淀,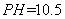 开始溶解,而
开始溶解,而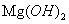 在
在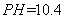 的时候开始沉淀,为了使
的时候开始沉淀,为了使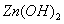 能完全析出不影响
能完全析出不影响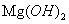 ,溶液的酸碱度控制在
,溶液的酸碱度控制在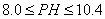 范围
范围
(5)a大理石粉难溶于水,选择熟石灰和烧碱溶液可以使溶液的碱性增强,有利于镁离子完全沉淀
(6)蒸发浓缩、冷却结晶能使晶体尽快的析出
(7)综合计算(不展开)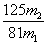
【答案】
(1) 增大反应物接触面积或增加反应时的接触面积,使反应更加充分。
(2) 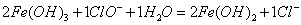
(3)  (或其他合理答案)
(或其他合理答案)
(4) 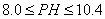 (或其他合理答案)
(或其他合理答案)
(5)b或(b和d);d
(6)蒸发浓缩、冷却结晶(或其他合理答案)
(7)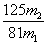 (或其他合理答案)
(或其他合理答案)


科目:高中化学 来源: 题型:
水热法制备Fe3O4纳米颗粒的总反应为:
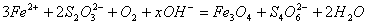 。下列说法正确的是( )
。下列说法正确的是( )
A.硫元素被氧化,铁元素被还原 B. Fe2+、S2O32-都是还原剂
C. x=2 D. 每生成1 mol Fe3O4,则转移电子数为3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
溴酸银(AgBrO3)溶解度随温度变化的曲线如图所示,下列说法错误的是( )
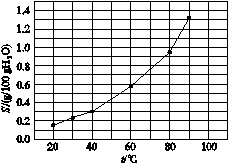
A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速率加快
C.60 ℃时溴酸银的Ksp约等于6×10-4
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
向27.2 g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5 L,固体物质完全反应,生成NO和Cu(NO3)2。在所得溶液中加入1.0 mol·L-1的NaOH溶液1.0 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2 g。下列有关说法不正确的是( )
A. Cu与Cu2O的物质的量之比为2∶1
B.硝酸的物质的量浓度为2.6 mol·L-1
C.产生的NO在标准状况下的体积为4.48 L
D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2 mol
(3)通过计算确定样品的组成(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
能在溶液中大量共存的一组离子是
A.NH4+ 、Ag+、PO43-、Cl- B.Fe3+、H+、I-、HCO3-
C.K+、Na+、NO3- 、MnO4- D.Al3+、Mg2+ 、SO42- 、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组用题27图装置探究氨的催化氧化.
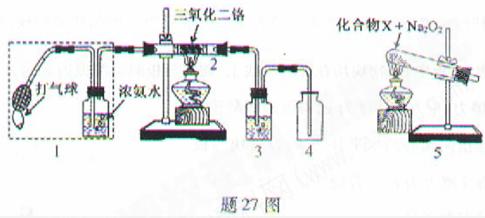
(1)氨催化氧化的化学方程式为___________________.
(2)加热玻璃管2一段时间后,挤压1中打气球鼓入空气,观察到2中物质呈红热状态;停止加热后仍能保持红热,该反应是_________反应(填“吸热”或“放热”).
(3)为保证在装置4中观察到红棕色气体,装置3应装入_________;若取消3,在4中仅观察到大量白烟,原因是___________________.
(4)为实现氨催化氧化,也可用装置5替换装置_________(填装置代号);化合物X为_ ________(只写一种),Na2O2的作用是___________________.
________(只写一种),Na2O2的作用是___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:
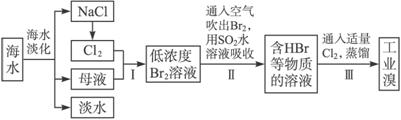
(1)请列举海水淡化的两种方法:__________________、__________________。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、_________、_________或H2、_________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为__________________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______________________。
(5)某化学研究性学习小组为 了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图:
了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图:
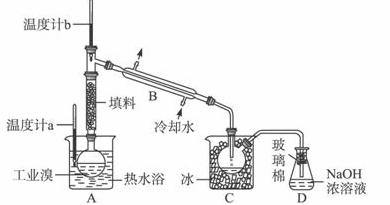
请你参与分析讨论:
①图中仪器B的名称:______________________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因为_______________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:_______________。
④C中液体产物颜色为_______________,为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列氧化还原反应中,水作为氧化剂的是
A.CO+H2O CO2+H2 B.3NO2+H2O=2HNO3+NO
CO2+H2 B.3NO2+H2O=2HNO3+NO
C.2Na2O2+2H2O=4NaOH+O2↑ D.2F2+2H2O=4HF+O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com