
标准状况下,mg气体A与ng气体B分子数相同,下列说法中不正确的是( )
|
| A. | 气体A与B的相对分子质量比为m:n |
|
| B. | 同质量气体A与B的分子个数比为n:m |
|
| C. | 同温同压下,同体积A气体与B气体的密度比为n:m |
|
| D. | 相同状况下,同体积A气体与B气体质量比为m:n |
| 阿伏加德罗定律及推论.. | |
| 专题: | 阿伏加德罗常数和阿伏加德罗定律. |
| 分析: | 标准状况下,分子数相同的气体A和B,它们的物质的量相同,气体体积相同. A、物质的量相同,相对分子质量之比等于质量之比. B、分子数之比与物质的摩尔质量成反比. C、同温同压,气体密度之比等于摩尔质量之比. D、相同状况下,同体积A气体与B气体物质的量相同,质量之比等于相对分子质量之比. |
| 解答: | 解:标准状况下,分子数相同的气体A和B,它们的物质的量相同,气体体积相同. A、由n=可知,分子数相同的气体,相对分子质量之比等于质量之比,即A与B相对分子质量之比为mg:ng=m:n,故A正确; B、A与B相对分子质量之比为m:n,同质量时由n=可知,分子数之比等于: =n:m,故B正确; C、同温同压,气体密度之比等于摩尔质量之比等于相对分子质量之比,即为m:n,故C错误; D、相同状况下,同体积的A与B的物质的量相同,则质量之比等于相对分子质量之比,即为m:n,故D正确. 故选:C. |
| 点评: | 本题考查阿伏伽德罗定律及其推论,明确同温、同压、同体积,则气体的分子数相同、物质的量相同及质量、物质的量、摩尔质量的关系是解答的关键,可借助PV=nRT理解. |


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
部分氧化的Fe—Cu合金样品(氧化产物为Fe2O3、CuO)共2.88g,经如下处理:

下列说法正确的是
A.滤液A中的阳离子为Fe2+、Fe3+、H+ B.V=224
C.样品中CuO的质量为2.0g D.样品中Fe元素的质量为1.07 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质及应用的说法正确的是
A.过量的铜与浓硝酸反应可生成NO
B. Fe在O2中的燃烧产物可用于制红色涂料
C. Na、Al、Cu可以分别用电解冶炼法、热还原法和热分解法得到
D.Fe2+、SO2都能使酸性高锰酸钾溶液褪色,前者表现出还原性后者表现出漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 1mol H2O的质量为18g/mol |
|
| B. | CH4的摩尔质量为16g |
|
| C. | 3.01×1023个SO2分子的质量为32g |
|
| D. | 标准状况下,1mol任何物质体积均为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图,在盛有溴水的三支试管中分别加入苯、四氯化碳和酒精,振荡后静置,出现下列现象,正确的结论是( )
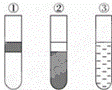
|
| A. | ①加入的是CCl4,②加入苯,③加酒精 | B. | ①加入的是酒精,②加入CCl4,③加苯 |
|
| C. | ①加入的是苯,②加入CCl4,③加酒精 | D. | ①加入的是苯,②加酒精,③加CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
取1.43g Na2CO3•10H2O溶于水配成100mL溶液,Na+ 物质的量浓度为 0.1mol/L ;取出20mL该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.004mol/L,加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略不计)为 230mL .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是
A.金属钠和水的反应:Na+2H2O=Na++ OH一+H2↑
B.向次氯酸钙溶液中通入SO2:
Ca2++2ClO-+H2O+SO2=CaSO3+2HClO
C.过量的铁与浓硝酸反应:Fe+6H++3NO3-=Fe3++3NO2↑+3H2O
D.过量的NaHSO4溶液与Ba(OH)2溶液反应:
2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
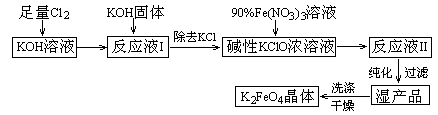 |

已知:① 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 →5KCl + KClO3 + 3H2O(条件:温度较高)
③ 2Fe(NO3)3 +3KClO+10KOH →2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
(1)该生产工艺应在温度 (填“较高”或“较低”)的情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)K2FeO4具有强氧化性的原因 ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度约为 。
(5)在“反应液I”中加KOH固体的目的是 (选填序号)。
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品 (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ca2+
B.用玻璃棒蘸取新制氯水,点在PH试纸的中央,与标准比色卡比较,测定氯水的PH
C.某溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝气体,说明原溶液中存在NH4+
D.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com