
| A. | 用1g 98%的浓硫酸加入4g水配制1:4硫酸溶液 | |
| B. | 配制2.0mo1•L-1硫酸溶液时,最后在容量瓶中加水稀释到标线,塞好盖子倒转摇匀后,发现液面低于标线 | |
| C. | 在100mL无水乙醇中,加人2g甲醛配制2%的甲醛洒精溶液 | |
| D. | 在80mL水中,加入18.4mol•L-1浓硫酸20mL,配制3.68mol•L-1稀硫酸 |
分析 A.硫酸溶液中,浓度越大其密度越大,根据质量和密度之间的关系确定其体积关系;
B.根据c=$\frac{n}{V}$来分析误差,如果n偏大或V偏小都导致配制溶液浓度偏高;
C.由于乙醇的密度为0.78g/mL,则所得溶液的质量小于100g;
D.硫酸溶液中,浓度越大其密度越大,根据c=$\frac{n}{V}$来分析溶液浓度.
解答 解:A.浓硫酸的密度大于1g/mL,水的密度是1g/mL,用1g98%的浓硫酸加4g水配成1:4(体积比)的硫酸,浓硫酸的体积和水的体积比小于1:4,导致配制溶液体积比偏小,故A错误;
B.配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇匀后,发现液面低于刻度线,溶质的物质的量和溶液的体积都不变,所以配制溶液浓度不变,故B错误;
C.由于乙醇的密度为0.78g/mL,故在100mL无水乙醇中加入2g甲醛,所得溶液的质量小于100g,则溶液的质量分数大于2%,故C正确;
D.浓硫酸溶液密度大于水的密度,在80mL水中加入18.4mol/L的硫酸20mL,溶液体积小于100mL,所以配制浓度高于3.68mol/L,故D正确;
故选CD.
点评 本题考查了化学实验方案的评价,侧重考查溶液配制方法及误差分析,题目难度中等,明确溶液配制方法为解答关键,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 维生素B5: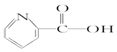 | B. | 阿司匹林: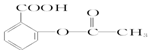 | ||
| C. | 芬必得: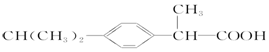 | D. | 摇头丸: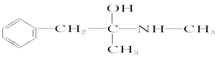 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ③ | C. | ②③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学方程式 | F2+H2?2HF | H2+Cl2?2HCl | H2+Br2(g)?2HBr | H2+I2(g)?2HI(g) |
| 平衡常数K(t1) | 1.8×1036 | 9.7×1012 | 5.6×107 | 43 |
| 平衡常数K(t2) | 1.9×1032 | 4.2×1011 | 9.3×106 | 34 |
| A. | 只有ab | B. | 只有abe | C. | 只有abce | D. | abcde |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
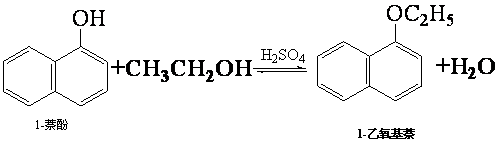
| 物质 | 相对分 子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醇 | |||||
| 1-萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
| 1-乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
| 乙醇 | 46 | 无色液体 | -114.1℃ | 78.5℃ | 任意比混溶 | |
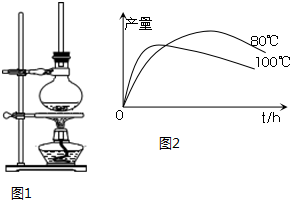
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应是放热反应还是吸热反应,由生成物与反应物的焓值差决定 | |
| B. | 升高温度,可以改变化学反应的反应热 | |
| C. | △H的大小与热化学方程式中的化学计量数无关 | |
| D. | 1 mol H2在足量Cl2中完全燃烧所放出的热量,是H2的燃烧热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com