
【题目】已知氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏 1 mol 氢气中的化学键消耗的能量为 ![]() kJ,破坏 1 mol 氯气中的化学键消耗的能量为
kJ,破坏 1 mol 氯气中的化学键消耗的能量为![]() kJ,形成 1 mol 氯化氢中的化学键释放的能量为
kJ,形成 1 mol 氯化氢中的化学键释放的能量为 ![]() kJ, 下列关系式中正确的是 ( )
kJ, 下列关系式中正确的是 ( )
A.![]() +
+![]() >
>![]() B.
B.![]() +
+![]() <
<![]() C.
C.![]() +
+![]() <2
<2![]() D.
D.![]() +
+![]() >2
>2![]()
【答案】C
【解析】
根据反应热△H=反应物的总键能-生成物的总键,计算该反应的反应热,氢气在氯气中燃烧,反应热△H<0,据此解答。
破坏1molH2中的化学键消耗的能量为Q1kJ,则HH键能为Q1kJ/mol;破坏1molCl2中的化学键消耗的能量为Q2kJ,则ClCl键能为Q2kJ/mol;形成1molHCl中的化学键释放的能量为Q3kJ,则HCl键能为Q3kJ/mol;对于H2(g)+Cl2(g)═2HCl(g),反应热△H=反应物的总键能生成物的总键能=Q1kJ/mol+Q2kJ/mol2Q3kJ/mol=(Q1+Q22Q3)kJ/mol,由于氢气在氯气中燃烧,反应热△H<0,即(Q1+Q22Q3)<0,所以Q1+Q2<2Q3。
答案为C。


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:高中化学 来源: 题型:
【题目】工业上可以通过电解NO2制备NH4NO3,其工作原理如图所示,下列说法正确的是
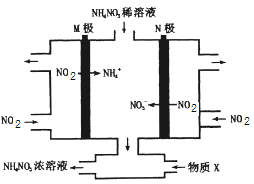
A. 电解过程中,阴极区NO2流入速率比阳极区NO2流入速率快些
B. 阴极区消耗1molNO2需补充6mol化合物X
C. 阳极反应为:NO2+e-+H2O=NO3-+2H+
D. 电解过程中,阴极区的pH小于阳极区的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用氯氧化法处理含氰(![]() )废水,一定条件下,氯气和
)废水,一定条件下,氯气和![]() 反应生成无毒气体。下列说法不正确的是
反应生成无毒气体。下列说法不正确的是
A. ![]() 中碳元素的化合价为+2
中碳元素的化合价为+2
B. 该反应的产物之一是无毒的![]()
C. 当1mol![]() 参与反应时,转移
参与反应时,转移![]()
D. 处理含0.1mol![]() 的废水,理论上需要消耗标准状况下
的废水,理论上需要消耗标准状况下![]() 的体积为5.6L
的体积为5.6L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验现象或图象信息不能充分说明相应的化学反应是放热反应的是( )
A | B | C | D | |
反应装置或图象 |
|
|
|
|
实验现象或图象信息 | 温度计的水银柱上升 | 反应物总能量大于生成物总能量 | 反应开始后,针筒活塞向右移动 | 反应开始后,甲处液面低于乙处液面 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用浓硫酸和乙醇制取乙烯,并验证探究乙烯与溴反应。实验装置如下(省略夹持、搅拌、加热装置)。
装置1 装置2
装置2 
请回答:
(1)仪器b的名称是_________;
(2)加热前,需将乙醇和浓硫酸混合。仪器a中盛装的是_________;
(3)乙醇制取乙烯的化学反应方程式为_________________;
(4)实验结果讨论:①甲同学观察到装置1中溴水颜色褪去,认为乙烯与溴水发生加成反应。化学反应方程式为____;
②乙同学观察到反应混合液逐渐变黑,认为乙烯中可能混有一种还原性气体,它也能使溴水颜色褪去。为证明乙烯能使溴水褪色,需将装置1虚线部分换成装置2,重做实验。装置2中,C所盛试剂是___;
③丙同学认为甲同学在观察实验现象时,漏掉一个能够证明乙烯与溴水发生了反应的重要实验现象。该现象是指_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中的氧化剂是_____,还原剂是____,每生成1molNa2FeO4转移_______mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用:_________。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42—、Cl-、H2O。写出并配平湿法制备高铁酸钾的离子反应方程式:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M、R、X、Y、Z为原子序数依次增大的短周期主族元素,M基态原子L层中p轨道电子数是s电子数的2倍,R是同周期元素中最活泼的金属元素,Y和M形成的一种化合物是引起酸雨的主要大气污染物,X的原子核外有3个单电子。请回答下列问题:
(1)R基态原子的电子排布式是______________,X、Y、Z电负性由小到大的顺序是_______(填元素符号)
(2)Y的氢化物在乙醇中的溶解度小于M的氢化物,其原因是______________
(3)在 H2O分子中,H﹣O﹣H的键角是_________,H3O+中H﹣O﹣H键角比H2O中H﹣O﹣H键角________填“大、小、相等”),原因为________________________________
(4)Y与M形成的YM3分子的空间构型是____________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是
A. 0.1 mol·L1NaOH溶液:Na+、K+、![]() 、
、![]()
B. 0.1 mol·L1FeCl2溶液:K+、Mg2+、![]() 、
、![]()
C. 0.1 mol·L1K2CO3溶液:Na+、Ba2+、Cl、OH
D. 0.1 mol·L1H2SO4溶液:K+、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒是人体必需的微量元素,右图是硒在周期表中的信息,关于硒元素的说法错误的是

A. 位于第四周期
B. 质量数为34
C. 原子最外层有6个电子
D. 相对原子质量为78.96
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com