
下列说法不正确的是
A.明矾能水解生成Al(OH)3胶体,可用作净水剂
B.水解反应NH +H2O
+H2O NH3·H2O+H+达到平衡后,升高温度平衡逆向移动
NH3·H2O+H+达到平衡后,升高温度平衡逆向移动
C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
D.盐类水解反应的逆反应是中和反应
科目:高中化学 来源: 题型:
氯化铜 (CuCl2·2H2O)中含FeCl2杂质。为制得纯净氯化铜晶体,首先将其制成水溶液, 然后按下面所示操作步骤进行提纯。
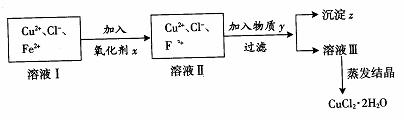
(1)加入氧化剂x的目的是
(2)下列氧化剂中最适合本实验的是
A.Cl2 B.KMnO4 C.NaClO D.H2SO4
(3)物质y和沉淀z的化学式分别是 和
查看答案和解析>>
科目:高中化学 来源: 题型:
氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制流程:

根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为________________________________。
(2)混合①中使用冰水的目的是________________________________。
(3)操作Ⅱ和操作Ⅲ的名称分别是________、________。
操作Ⅲ一般适用于分离________混合物。(选填编号)
a.固体和液体 b.固体和固体
c.互不相溶的液体 d.互溶的液体
(4)混合②中加入Na2SO3的目的是________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色,于是甲乙丙同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为________,若假设成立,可观察到的现象为________。乙同学假设工业氢溴酸呈淡黄色是因为________,其用于证明该假设所用的试剂为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)当水蒸气通过红热的铁时,反应的化学方程式为__________________________,在反应中铁元素化合价______,发生__________反应,铁表现出较强的____________。若有8.4g铁发生反应,则生成氢气标准状况下的体积是 L。
(2)因为多数金属单质有较强的____________,所以自然界中的大多数金属以____________态存在,只有极少数极不活泼的金属如____________等以____________态存在。
查看答案和解析>>
科目:高中化学 来源: 题型:
对滴有酚酞试液的下列溶液,操作后颜色变深的是
A.明矾溶液加热
B.CH3COONa溶液加热
C.氨水中加入少量NH4Cl固体
D.小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学实验小组对以下四种物质的水溶液,加热蒸干并灼烧,最终不能得到该物质固体的是
①氯化铁 ②碳酸钠 ③硫酸亚铁 ④硅酸钠
A.仅①③ B.仅②④
C.仅①③④ D.仅①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是____________________________________________
________________________________________________________________________
(用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH )________(填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH
)________(填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH )。
)。
(3)如图是0.1 mol·L-1电解质溶液的pH随温度变化的图像。

①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是________(填写字母),导致pH随温度变化的原因是__________________________________________________________;
②20 ℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO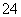 )-c(NH
)-c(NH )-3c(Al3+)=________。
)-3c(Al3+)=________。
(4)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:

试分析图中a、b、c、d四个点,水的电离程度最大的是________;在b点,溶液中各离子浓度由大到小的排列顺序是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y均是由C、H 、O三种元素组成的相对分子质量小于240的芳香族化合物,已知:
、O三种元素组成的相对分子质量小于240的芳香族化合物,已知:
Ⅰ.化合物X、Y中三种元素C、H、O的质量比均为9∶1∶3;
Ⅱ.X、Y互为同分异构体,且X、Y均可以发生下列化学反应:
X+H2O A1+B1(
A1+B1( C5H12O)
C5H12O)
Y+H2O A2+B2
A2+B2
B1和B2互为同系物,B1、B2的相对分子质量的关系为Mr(B1)-Mr(B2)=42。
(1)X或Y的分子式是____________。
(2)A1的分子式是________;A1能够发生的化学反应有________(填序号)。
①酯化反应 ②氧化反应 ③与三氯化铁溶液发生显色反应 ④消去反应 ⑤与溴水发生取代反应 ⑥与溴水发生加成反应
(3)A2与浓硫酸共热可以发生消去反应,也可以在铜作催化剂的条件下被氧气氧化,其氧化产物与新制的氢氧化铜悬浊液共热生成的有机物苯环上的一氯代物只有一种。
①Y的结构简式为______________________________________________;
②A2与浓硫酸共热发生消去反应的化学方程式为___________________________________
_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com