
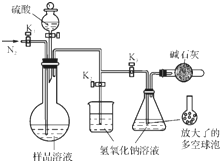
 碳酸钠-过氧化氢加合物(aNa2CO3•bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:
碳酸钠-过氧化氢加合物(aNa2CO3•bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:分析 (1)第1步中,稳定剂与水反应生成2种常见的难溶物,则生成氢氧化镁和硅酸;
(2)反应保持为15℃左右,可采取15℃水浴;
(3)降低碳酸钠过氧化氢加合物的溶解度;
(4)①配制250mL一定物质的量浓度的溶液,需要250 mL容量瓶、烧杯、玻璃棒、胶头滴管等;
②滴定终点时高锰酸钾溶液元素不褪去;
(5)①根据仪器的感量与量取溶液的体积选取仪器;
②为确保生成的二氧化碳被氢氧化钠溶液完全吸收应防止漏气,且使仪器中的二氧化碳都进入氢氧化钠溶液中;
③为获得样品中碳酸钠的含量,还要知道氢氧化钠溶液的浓度.
解答 解:(1)第1步中,稳定剂与水反应生成2种常见的难溶物,则生成氢氧化镁和硅酸,根据元素守恒知,还生成氯化钠,根据反应物和生成物知,该反应方程式为:MgCl2+Na2SiO3+2H2O=2NaCl+Mg(OH)2↓+H2SiO3↓,
故答案为:MgCl2+Na2SiO3+2H2O=2NaCl+Mg(OH)2↓+H2SiO3↓;
(2)反应保持为15℃左右,可采取15℃水浴,水浴加热时,受热均匀,便于控制温度,
故答案为:15℃水浴;
(3)根据相似相溶原理知,碳酸钠-过氧化氢在有机溶剂中的溶解度较小,利用酒精洗涤,可以降低碳酸钠-过氧化氢的溶解度,有利于晶体的析出,减少损失,有利于干燥
故答案为:降低碳酸钠-过氧化氢化合物的溶解度,有利于晶体析出;
(4)①在烧杯中溶解,并用玻璃棒搅拌,移入250mL容量瓶中,加水并用胶头滴管定容,
故答案为:250 mL容量瓶、胶头滴管;
②当溶液呈浅红色且30 s内不褪色时达到滴定终点,
故答案为:溶液呈浅红色且30 s内不褪色;
(5)①准确移取40.00mL氢氧化钠溶液需要的仪器是碱式滴定管,故答案为:碱式滴定管;
②步骤1~7中,确保生成的二氧化碳被氢氧化钠溶液完全吸收的实验步骤有:防止漏气,为防止烧瓶中溶液溶解二氧化碳,要将溶液加热,为防止烧瓶中含有二氧化碳,用氮气将烧瓶内的二氧化碳赶到氢氧化钠溶液,
故选:1,5,6;
③为获得样品中碳酸钠的含量,还需要知道氢氧化钠的浓度,所以还需补充的实验是:用H2SO4标准溶液标定NaOH溶液的浓度,
故答案为:用H2SO4标准溶液标定NaOH溶液的浓度.
点评 本题考查制备实验方案,涉及滴定实验、仪器的选取、物质分离和提纯、对操作与原理的分析评价等,明确实验原理及实验基本操作、物质性质是解本题关键,同时考查学生的分析问题、解决问题的能力,难度中等.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:填空题
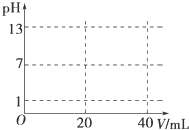 溶液中的化学反应大多是离子反应.根据要求回答下列问题.
溶液中的化学反应大多是离子反应.根据要求回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

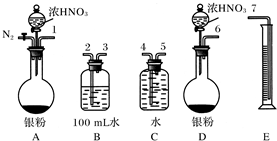
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 65g锌与足量稀硫酸反应产生的气体体积为22.4L | |
| B. | 标准状况下,以任意比混合的H2和CO气体共8.96L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2NA | |
| C. | 0.2mol H2O2在MnO2催化下充分反应生成O2的数目为0.2NA | |
| D. | 同温同压下,1mol H2在空气中充分燃烧,消耗O2的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe( NO3)3溶液中加入过量HI溶液:2Fe3++2I-═2Fe2++I2 | |
| B. | 浓烧碱溶液中加入铝片:2A1+2OH-═2AlO2-+H2 | |
| C. | H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4+H2O | |
| D. | 将新制氢氧化铜悬浊液加入氨水中:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++2OH-+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| B. | NaHCO3溶液中加入HCl:CO32-+2H+═CO2↑+H2O | |
| C. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- | |
| D. | “84消毒液”和“洁厕灵”(主要成分为盐酸)混合使用会产生有毒气体:$ClO_3^-$+5Cl-+6H+═3Cl2↑+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 将Al投入到烧碱溶液中:2Al+2OH-═AlO2-+2H2O | |
| C. | 将Al(OH)3投入到烧碱溶液中:Al(OH)3+OH-═AlO2-+2H2O | |
| D. | 向NaHCO3溶液中加入适量KOH溶液:HCO3-+OH-═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入合金的质量不可能为6.6g | |
| B. | 参加反应的硝酸的物质的量浓度为1mol/L | |
| C. | 生成沉淀完全时消耗NaOH溶液的体积为100 mL | |
| D. | 生成NO气体体积为2.24 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com