
| A. | 化学反应速率关系是:2υ正(NH3)=3υ正(H2O) | |
| B. | 达到化学平衡时,4υ正(O2)=5υ逆(NO) | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
分析 反应中反应速率之比等于化学计量数之比,达到平衡时,正逆反应速率相等,增大压强,浓度增大,正逆反应速率都增大,以此解答该题.
解答 解:A.反应速率之比等于化学计量数之比,应为3υ正(NH3)=2υ正(H2O),故A错误;
B.4υ正(O2)=5υ逆(NO),可说明正逆反应速率相等,达到化学平衡状态,故B正确;
C.增大压强,浓度增大,正逆反应速率都增大,故C错误;
D.无论是否达到平衡状态,都存在单位时间内生成x mol NO的同时,消耗x mol NH3,故D错误.
故选B.
点评 本题考查化学平衡状态的判断、化学平衡移动的方向以及影响因素,为高频考点,侧重于双基的考查,注意知识的归纳和整理,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 分解反应 | B. | 置换反应 | C. | 复分解反应 | D. | 化合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
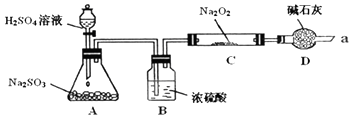
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCl2═Ca2++Cl2 | B. | H2SO4═2 H++SO42- | ||
| C. | Ba(OH)2═Ba++2OH- | D. | NaHCO3═Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 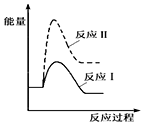 | B. | 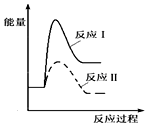 | ||
| C. | 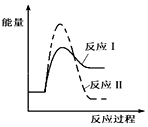 | D. | 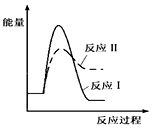 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 26g | B. | 36g | C. | 104g | D. | 37.8g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
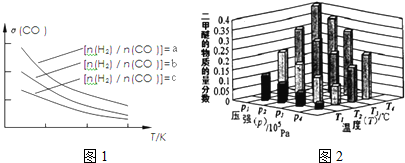
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 容器内气体压强保持不变 | |
| B. | 吸收ymolH2只需1 mo1MHx | |
| C. | 若向容器内通入少量氢气,则V(放氢)>V(吸氢) | |
| D. | 若降温,该反应的平衡常数增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com