

 (B2H6为乙硼烷)
(B2H6为乙硼烷) ).F的结构简式是
).F的结构简式是| 8.96L |
| 22.4L/mol |
| 9g |
| 18g/mol |
| 0.4mol |
| 0.1mol |
| 0.5mol×2 |
| 0.1mol |
 .F可以与Cu(OH)2反应,含有醛基,1mol F与2mol H2反应生成I(
.F可以与Cu(OH)2反应,含有醛基,1mol F与2mol H2反应生成I( ,则应含有碳碳双键,则F的结构简式为
,则应含有碳碳双键,则F的结构简式为 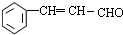 ,F中醛基氧化为羧基生成G为
,F中醛基氧化为羧基生成G为 ,G与E发生酯化反应生成H为
,G与E发生酯化反应生成H为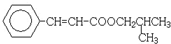 ,据此解答.
,据此解答.| 8.96L |
| 22.4L/mol |
| 9g |
| 18g/mol |
| 0.4mol |
| 0.1mol |
| 0.5mol×2 |
| 0.1mol |
 .F可以与Cu(OH)2反应,含有醛基,1mol F与2mol H2反应生成I(
.F可以与Cu(OH)2反应,含有醛基,1mol F与2mol H2反应生成I( ,则应含有碳碳双键,则F的结构简式为
,则应含有碳碳双键,则F的结构简式为 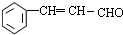 ,F中醛基氧化为羧基生成G为
,F中醛基氧化为羧基生成G为 ,G与E发生酯化反应生成H为
,G与E发生酯化反应生成H为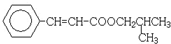 ,
, ,则应含有碳碳双键,则F的结构简式为
,则应含有碳碳双键,则F的结构简式为 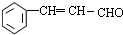 ,故答案为:
,故答案为: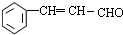 ;
; ,
, ,
, ;
; ;
; )具有相同官能团的G的芳香类同分异构体,含有碳碳双键、-COOH,符合条件的结构简式:
)具有相同官能团的G的芳香类同分异构体,含有碳碳双键、-COOH,符合条件的结构简式: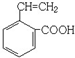 、
、 、
、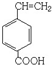 、
、 ,
, 、
、 、
、 、
、 .
.


科目:高中化学 来源: 题型:
| A、与硅相比,金刚石的硬度大,熔点高 |
| B、HF、HCl、HBr、HI热稳定性依次减弱 |
| C、F2、Cl2、Br2、I2的沸点逐渐升高 |
| D、F2比O2更容易与H2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
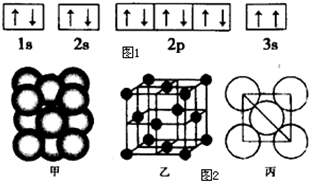 现有七种元素,其中A.B.C.D.E为短周期主族元素,F.G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
现有七种元素,其中A.B.C.D.E为短周期主族元素,F.G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.| A原子的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol,I2=1451kJ/mol,I3=7733kJ/mol,I4=10540kJ/mol, |
| D原子核外所有P轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
查看答案和解析>>
科目:高中化学 来源: 题型:
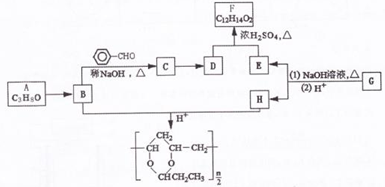
| 稀NaOH |
| △ |
 +H2O(R、R′表示烃基或氢)
+H2O(R、R′表示烃基或氢)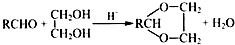
查看答案和解析>>
科目:高中化学 来源: 题型:
 根据Fe3++Ag?Fe2++Ag+,可用Fe3+做刻蚀液将试管中的银镜洗去.
根据Fe3++Ag?Fe2++Ag+,可用Fe3+做刻蚀液将试管中的银镜洗去.- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有OH-的溶液 |
| B、c(OH-)>c(H+)的溶液 |
| C、c(OH-)>1×10-7mol?L-1的溶液 |
| D、滴入酚酞后显无色的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com