
【题目】按要求填空:
(1)质量数为37的氯原子符号为_______。
(2)S2-的结构示意图为______。
(3)氮原子的电子式为______,N2的电子式为______,NH4+的电子式为_________
(4)磷原子的核外电子排布式为______,其价电子排布式为_____, 其价电子排布图为_____。
【答案】 3717Cl(或37Cl) 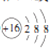
![]()
![]()
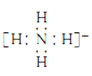 1s22s22p63s23p3{或[Ne]3s23p3} 3s23p3
1s22s22p63s23p3{或[Ne]3s23p3} 3s23p3 ![]()
【解析】(1)Cl的质子数为17,质量数为37,则质量数为37的氯原子符号为![]() 或37Cl;故答案为:
或37Cl;故答案为: ![]() 或37Cl
或37Cl
(2)硫离子最外层得到两个电子达到8电子稳定结构,所以其结构示意图为:![]() ;故答案为:
;故答案为:![]()
(3)氮原子最外层有5个电子,有一对孤对电子,氮原子的电子式为:![]() ;氮气分子的电子式为
;氮气分子的电子式为![]() ;NH4+的电子式为
;NH4+的电子式为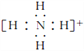 ;故答案为:
;故答案为:![]() 、
、![]() 、
、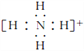
(4)磷元素核外有15个电子,根据书写规则知有3层,s轨道最多容纳两个电子,p轨道最多容纳6个电子,所以磷原子的核外电子排布式为1s22s22p63s23p3或[Ne]3s23p3;价电子为最外层的电子数,所以排布为3s23p3;价电子排布图也要顾及先向上排满,再排向下;所以排布图为:![]() 。故答案为:1s22s22p63s23p3或[Ne]3s23p3 、 3s23p3 、
。故答案为:1s22s22p63s23p3或[Ne]3s23p3 、 3s23p3 、 ![]()


科目:高中化学 来源: 题型:
【题目】下列各组离子中,因发生氧化还原反应而不能大量共存的是( )
A.K+、H+、Fe2+、MnO4﹣
B.Fe3+、Ba2+、SO42﹣、NO3﹣
C.Al3+、Na+、SO42﹣、CO32﹣
D.Fe3+、H+、SO42﹣、ClO﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家正在研究温室气体CH4、CO2的转化和利用。
(1)在Ni基催化剂的作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni外围价电子中有_________对成对电子。
②CH4、CO2、H2分子中有孤对电子的是_________.
(2)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数如下表。CH4与H2O形成的水合物俗称“可燃冰”。
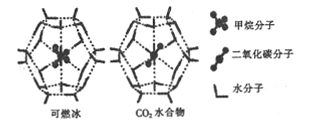
参数 分子 | 分子直径/mm | 分子与H2O的结合能(E) |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | y |
①CO2水合物分子间存在的两种作用力是___________.
②为开采深海海底的“可燃冰”,科学家已经证明可用CO2置换CH4。已知上图中笼状结构的空腔直径为xnm,根据上述图表,从物质的结构与性质的角度分析:x_____0.512;y_______16.40。(填“>”“<"或“=”)
③写出CH4的一种等电子体: __________;SiO2与CO2是否互为等电子体?_________(填“是”或“不是”),理由是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环扁桃酯具有松弛血管平滑肌、扩张血管的功能,其结构简式如下图。下列对该物质的叙述中,正确的是
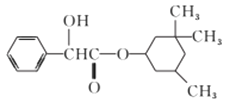
A. 该有机物苯环上的二氯代物共有8种
B. 该有机物分子中至少有7个碳原子共平面
C. 该有机物可以与Br2的CCl4溶液发生加成反应使之褪色
D. 1mol该有机物最多可与2molNaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的钙离子、镁离子、硫酸根离子及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)第①步中,操作A是__________,第⑤步中,操作B是__________。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)____________________________。
(3)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因是_________________________。
(4)判断氯化钡已过量的方法是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com