
【题目】下列关于有机物的说法或表述中不正确的是
A.等质量的乙烷、乙烯、乙炔在氧气中完全燃烧,消耗的氧气乙烷最多
B.可借助于核磁共振氢谱区分乙醇和二甲醚这两种物质
C.CH3CH(CH3)CH(CH3)CH(C2H5)CH2CH3的名称:2,3-二甲基-4-乙基己烷
D.石油裂解和油脂的皂化都是高分子生成小分子的过程
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ、制取氨气并完成喷泉实验(图中夹持装置均已略去)。
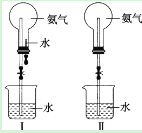
(1)写出实验室制取氨气的化学方程式______。
(2)收集氨气应使用______法,要得到干燥的氨气可选用作干燥剂______。
(3)如果只提供如图Ⅱ所示装置,请说明引发喷泉的方法是______。
Ⅱ.下图是甲、乙两位同学探究铜与稀硝酸反应还原产物的实验装置图,请回答下列问题:
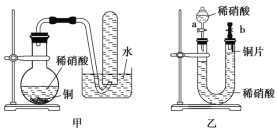
(1)写出铜和稀硝酸反应的离子方程式:______。
(2)实验装置甲能否证明铜和稀硝酸反应的产物是 NO 气体______(填“能”或“不能”),请简述理由(用文字和化学方程式表示):______。
(3)若用实验装置乙进行实验,检查装置气密性的操作是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氮可由NO和O2生成,已知在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g) 2NO2(g) ΔH, n(NO)、n(O2)随时间的变化如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
n(O2)/mol | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
(1)该反应的化学平衡常数表达式为K=___________________
(2)已知:K800 ℃>K1 000 ℃,则该反应的ΔH_________0(填“大于”或“小于”),
(3)用O2表示0~2 s内该反应的平均速率为_________。
(4)能说明该反应已达到平衡状态的是_________。
a.容器内气体颜色保持不变 b.2υ逆(NO)=υ正(O2)
c.容器内压强保持不变 d.容器内气体密度保持不变
(5)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动,应采取的措施有____。
A.升温 B.加入氧气 C. 降温 D.增大压强
(6)在800 ℃时,计算通入2 mol NO和1 mol O2的平衡常数K=_________
(7)已知下列反应在某温度下的平衡常数以及ΔH
H2(g)+S(s) H2S(g) K1 ΔH1
S(s)+O2(g) SO2(g) K2 ΔH2
则在该温度下反应H2(g)+SO2(g) O2(g)+H2S(g) K3 ΔH3
平衡常数K3=__________(用含有K1 K2的式子表示);
其反应热ΔH3=________(用含有ΔH1 ΔH2的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用![]() 溶液分别滴定
溶液分别滴定![]() 的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是
的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是![]()
![]()

A.Ⅱ表示的是滴定醋酸的曲线
B.![]() 时,滴定醋酸消耗的
时,滴定醋酸消耗的![]() 小于
小于![]()
C.![]() 时,两份溶液中
时,两份溶液中![]()
D.![]() 时,醋酸溶液中
时,醋酸溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL无色溶液可能含有Na+、NH4+、Mg2+、Al3+、Fe3+、CO32-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)
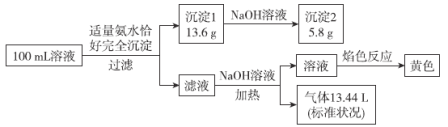
下列说法错误的是( )
A.原溶液一定存在Na+、NH4+、Mg2+、Al3+和Cl-,一定不存在Fe3+、CO32-
B.原溶液中c(NH4+)=1mol·L-1
C.沉淀2的成分为Mg(OH)2
D.原溶液中c(Cl-)≥6mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十氢萘(C10H18)是一种优秀的液体储氢材料,其高压催化脱氢得到四氢萘(C10H12),可用于燃料电池汽车。已知:①C10H18(l) ![]() C10H12(l)+3H2(g) △H1②C10H12(l)
C10H12(l)+3H2(g) △H1②C10H12(l)![]() C10H8(l)+2H2(g) △H2。一定温度下,在1L恒容密闭容器中进行C10H18(1.000mol)高压催化脱氢实验,测得C10H12和C10H8的物质的量随时间变化关系如图1所示,上述反应的“能量—反应过程”如图2所示。
C10H8(l)+2H2(g) △H2。一定温度下,在1L恒容密闭容器中进行C10H18(1.000mol)高压催化脱氢实验,测得C10H12和C10H8的物质的量随时间变化关系如图1所示,上述反应的“能量—反应过程”如图2所示。
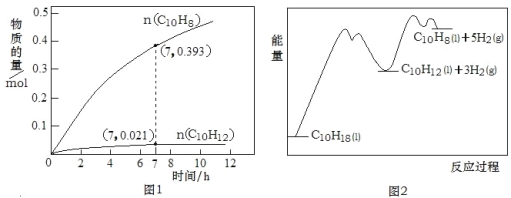
下列判断正确的是( )
A. 反应至7h时,C10H18的转化率为2.1%
B. 在7h时,反应体系中氢气的物质的量为0.849mol
C. 反应①的活化能高于反应②的活化能
D. △H2>△H1>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
科目:高中化学 来源: 题型:
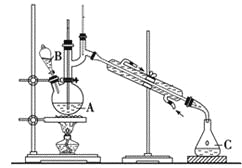
【题目】某实验小组利用如下装置合成化工原料正丁醛。发生的反应如下:
![]()
反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.810 9 | 微溶 |
正丁醛 | 75.7 | 0.801 7 | 微溶 |
实验步骤如下:
将6.0 g Na2Cr2O7放入100 mL烧杯中,加30 mL水溶解,再缓慢加入5 mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0 g正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95 ℃,在C中收集90 ℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,再将有机层干燥、蒸馏后得正丁醛2.0 g。
回答下列问题:
(1)实验中不能将Na2Cr2O7溶液加到浓硫酸中的理由是_____________________。
(2)加入沸石的作用是_________________。
(3)分液漏斗使用前必须进行的操作是__________________。
(4)反应温度应保持在90~95℃,其原因是___________________。
(5)本实验中,正丁醛的产率为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S粗品含有杂质,其纯化、含量测定方法如下。回答下列问题:
(1)粗品经水浸、过滤、__________________、洗涤、干燥等操作可以除去不溶性杂质,得到较纯的Na2S固体。
(2)国标中采用如图所示装置测定Na2S样品溶液中Na2CO3的百分含量(实验前,吸收管1、吸收管2、参比管中均装入组成相同的乙醇、丙酮混合溶液,该溶液吸收CO2后,颜色发生改变) 。
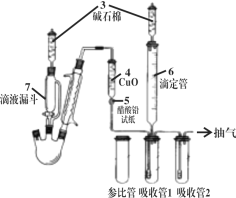
(步骤一)标定KOH标准溶液
准确称取w g邻苯二甲酸氢钾(KC8H5O4,摩尔质量为M g/mol)置于锥形瓶中,加入适量蒸馏水、2滴指示剂,用待标定的KOH溶液滴定至终点,消耗v mL KOH溶液。
①标定过程中应该选用的指示剂名称是______,理由是__________;
(已知邻苯二甲酸的电离平衡常数为Ka1=1.1×10-3,Ka2=4.0×10-6)
②KOH溶液的准确浓度为_____mol/L(用含M、v、w的代数式表示)
(步骤二)往三颈烧瓶中先后加入100mL 样品溶液、15 ml过氧化氢溶液(足量),连接好装置,加热并打开抽气装置;
(步骤三)上述反应完成后,从滴液漏斗中慢慢加入足量稀硫酸溶液,充分反应;
(步骤四)用装置6中的KOH标准溶液滴定吸收管1中的溶液至与参比管中溶液相同的颜色,3 min内不变色为终点。
③过氧化氢的作用是______;碱石棉的作用是__________;
④如果抽气速度过快,可能导致测定结果_________(填“偏高”、“偏低”或“无影响”);
⑤若步骤三中出现_______________________(填现象),说明实验失败,必须重新测定。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com