
【题目】下列物质①HCl②CO2③H2O④H2⑤NaHSO4⑥Cl2⑦NaF⑧CH4⑨CaO⑩MgCl2
(1)属于离子化合物的是_______,只含共价键的是______,既含有离子键又有共价键的是______。
(2)属于电解质的是__________,属于非电解质的是___________。
(3)将NaHSO4熔化,破坏了NaHSO4中的__________键,写出其电离方程式_____________。将NaHSO4溶于水,破坏了NaHSO4中的_________键,写出其电离方程式_____________。
(4)分别用电子式表示氯化镁、氯气的形成过程:____________。
【答案】(1)⑤⑦⑨⑩;①②③④⑥⑧;⑤
(2)①③⑤⑦⑨⑩;②⑧
(3)离子;NaHSO4=Na++HSO4-;离子键和共价键;NaHSO4=Na++H++SO42-
(4)![]() ;
;![]()
【解析】
试题分析:①HCl分子中只含有共价键,属于共价化合物;在水中能完全电离出自由移动的阴阳离子,属于强电解质;②CO2分子中只含有共价键,属于共价化合物;在水中自身不能电离出自由移动的阴阳离子,属于非电解质;③H2O分子中只含有共价键,属于共价化合物;能发生微弱的电离生成氢离子和氢氧根离子,属于弱电解质;④H2分子中只含有共价键,属于单质,所以既不是电解质也不是非电解质;⑤NaHSO4中钠离子和硫酸氢根离子间存在离子键、硫酸氢根离子内存在极性共价键,属于离子化合物;在水中及融化状态下均能完全电离出自由移动的阴阳离子,属于强电解质;⑥Cl2分子中只含有共价键,属于单质,所以既不是电解质也不是非电解质;⑦NaF中钠离子和氟离子间只存在离子键、属于离子化合物;在水中及融化状态下均能完全电离出自由移动的阴阳离子,属于强电解质;⑧CH4分子中只含有共价键,属于共价化合物;在水中自身不能电离出自由移动的阴阳离子,属于非电解质;⑨CaO中钠离子和氧离子间只存在离子键、属于离子化合物;在融化状态下能完全电离出自由移动的阴阳离子,属于强电解质;⑩MgCl2中镁离子和氯离子间只存在离子键、属于离子化合物;在水中及融化状态下均能完全电离出自由移动的阴阳离子,属于强电解质。据此可得下列结论:
(1)属于离子化合物的是⑤⑦⑨⑩,只含共价键的是①②③④⑥⑧,既含有离子键又有共价键的是⑤。
(2)属于电解质的是①③⑤⑦⑨⑩,属于非电解质的是②⑧。
(3)将NaHSO4熔化,破坏了NaHSO4中的离子键,其电离方程式为:NaHSO4=Na++HSO4-。将NaHSO4溶于水,破坏了NaHSO4中的离子键和部分共价键,其电离方程式为:NaHSO4=Na++H++SO42-。
(4)镁是活泼的金属元素、氯是活泼的非金属元素,二者发生反应过程中进行电子得失生成离子化合物氯化镁,其形成过程可表示为:![]() ;两个氯原子通过共价键形成氯气分子,其形成过程可表示为:
;两个氯原子通过共价键形成氯气分子,其形成过程可表示为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是 ( )
A. 催化剂能够改变化学反应路径 B. 升高温度提高了活化分子百分数
C. 增大反应物浓度提高了活化分子百分数 D. 增大压强能增大活化分子的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是( )

A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质X逐渐加入(或滴入)Y溶液中,其生成沉淀的物质的量与加入X的物质的量关系如图所示,符合图示情况的是( )
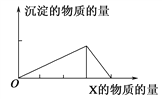
A | B | C | D | |
X | NaOH | HCl | CO2 | AlCl3 |
Y | AlCl3 | NaAlO2 | Ca(OH)2 | NaOH |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质发生变化时,所克服的微粒间作用力属于同种类型的是( )
A.二氧化硅和氢氧化钠的熔化
B.碘和干冰的升华
C.氯化氢和氯化钠的溶解
D.汞和硫的气化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.6 kJ·mol-1。
2NH3(g) ΔH=-92.6 kJ·mol-1。
实验测得起始、平衡时的有关数据如下表所示:
容器 编号 | 起始时各物质的物质的量/mo | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15 kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述错误的是
A.容器①、②中反应的平衡常数相等
B.容器②中达平衡时放出的热量Q=23.15 kJ
C.若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
D.平衡时,两个容器中NH3的体积分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中10种元素用元素符号或化学式填空回答以下问题:

Ⅰ.填写下列空白:
(1)非金属性最强的元素是___________(填元素符号),
(2)写出①与③形成原子个数比为1:1化合物的电子式:____________,该化合物酸性条件下与高锰酸钾反应的离子方程式:__________________________
(3)最高价氧化物对应的水化物中碱性最强的是_______(填化学式),写出该物质与⑦的最高价氧化物对应的水化物反应的离子方程式为:____________。
(4)由①②③⑩四种元素中的三种组成的一种强酸,该强酸的稀溶液与铜反应的离子方程式 ____________________________
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图中的变化,其中A是一种淡黄色固体,可作供氧剂,X是一种氢化物,常温下为液体。则:

(1)A与液体X反应的化学方程式:____________________________;
(2)气体Y是一种大气污染物,无色、有刺激性气味的气体,直接排放会形成酸雨。写出气体Y与氯水反应的离子方程式:___________________________;
(3)在100 mL 18 mol/L的F浓溶液中加入过量铜片,加热使之充分反应,产生气体的体积为11.2 L(标况下),则反应过程中转移的电子数为__________(用“NA”表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:

下列说法中正确的是
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com