
【题目】CMU是一种荧光指示剂,可通过下列反应制备:
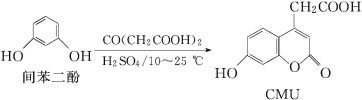
下列说法正确的是( )
A.1 mol CMU最多可与4 mol Br2反应
B.1 mol CMU最多可与4 mol NaOH反应
C.可用FeCl3溶液鉴别间苯二酚和CMU
D.CMU在酸性条件下的水解产物只有1种
【答案】BD
【解析】
A. ![]() 中碳碳双键可与溴(
中碳碳双键可与溴(![]() )发生加成反应,酚羟基(
)发生加成反应,酚羟基(![]() )邻位
)邻位![]() 原子可被
原子可被![]() 取代;
取代;
B. ![]() 中能与氢氧化钠(
中能与氢氧化钠(![]() )反应的为酚羟基(
)反应的为酚羟基(![]() )、羧基(
)、羧基(![]() )以及酯基(
)以及酯基(![]() );
);
C. 间苯二酚和![]() 都含有酚羟基(
都含有酚羟基(![]() );
);
D. ![]() 含有酯环,水解产物只有一种。
含有酯环,水解产物只有一种。
A. ![]() 中碳碳双键可与溴(
中碳碳双键可与溴(![]() )发生加成反应,酚羟基(
)发生加成反应,酚羟基(![]() )邻位H原子可被
)邻位H原子可被![]() 原子取代,则
原子取代,则![]() 最多可与
最多可与![]() 反应,故A错误;
反应,故A错误;
B. ![]() 中能与氢氧化钠发生反应的官能团为:酚羟基(
中能与氢氧化钠发生反应的官能团为:酚羟基(![]() )、羧基(
)、羧基(![]() )以及酯基(
)以及酯基(![]() ),酯基(
),酯基(![]() )可水解生成酚羟基(
)可水解生成酚羟基(![]() )和羧基(
)和羧基(![]() ),则
),则![]() 最多可与
最多可与![]() 反应,故B正确;
反应,故B正确;
C. 与![]() 溶液反应显紫色的是酚羟基(
溶液反应显紫色的是酚羟基(![]() ),间苯二酚和
),间苯二酚和![]() 都含有酚羟基,可与氯化铁反应显紫色,不能鉴别,C错误;
都含有酚羟基,可与氯化铁反应显紫色,不能鉴别,C错误;
D. ![]() 含两个环,且一个为酯环,在酸性条件下的水解,水解产物有一种,D正确。
含两个环,且一个为酯环,在酸性条件下的水解,水解产物有一种,D正确。


科目:高中化学 来源: 题型:
【题目】请回答下列问题:
Ⅰ.一定条件下,A(g)+B(g) ![]() C(g) ΔH<0,达到平衡后根据下列图象判断:
C(g) ΔH<0,达到平衡后根据下列图象判断:
A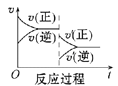 B
B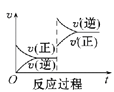 C
C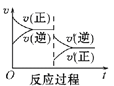 D
D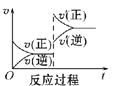
(1)升高温度,达到新平衡的是_____(选填字母),新平衡中C的体积分数______(选填“增大”“减小”或“不变”)。
(2)减小压强,达到新平衡的是________(选填字母),A的转化率________(选填“增大”“减小”或“不变”)。
Ⅱ. 取五等份NO2,分别充入五个温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g) ![]() N2O4(g) ΔH<0,反应一段时间后,分别测定体系中NO2的体积分数,并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是___。
N2O4(g) ΔH<0,反应一段时间后,分别测定体系中NO2的体积分数,并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是___。
①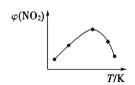 ②
②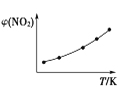 ③
③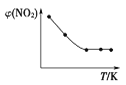 ④
④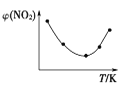
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①锌跟稀硫酸反应制H2,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白口铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,把氧化铝加入液态冰晶石中熔融后电解
⑤钢铁表面常易腐蚀生成Fe2O3·nH2O
A.全部B.①③④⑤C.①②⑤D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据要求填空:
(1)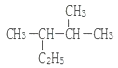 用系统命名法命名:______________;
用系统命名法命名:______________;
(2)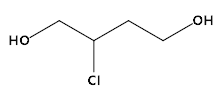 的分子式______________;
的分子式______________;
(3) ![]() 官能团的名称是________________。
官能团的名称是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用作食品添加剂(抗结剂),我国卫生部规定实验中黄血盐的最大使用量为10mg/kg。一种制备黄雪盐的工艺如下:

回答下列问题:
(1)步骤Ⅰ反应的化学方程式为__________________________。
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为____________(填化学式)。
(3)步骤Ⅴ所用的试剂X是___________。(填化学式)
(4)工艺中用到剧毒的HCN溶液,含CN- 的废水必须处理后才能排放。
已知: HCN是一种具有苦杏仁味的无色剧毒液体,易挥发,25℃时Ka(HCN)=6.25×10-10;溶液中H2CO3、HCO3-、CO32-的存在与溶液pH的关系如图所示:
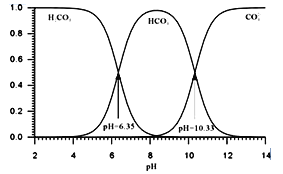
①NaCN的电子式为___________。
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5~8.5,用NaClO溶液完全氧化OCN-生成N2和两种盐。第一步控制强碱性的主要目的是_______,第二步反应的离子方程式为____________。
(5)已知蓝色染料普鲁士蓝的合成方法如下:

用硫酸亚铁碱性试纸可以检验食品中是否含有CN-,方案如下:

若试纸变蓝则证明食品中含有CN-,基于普鲁士蓝的合成原理,请解释检测时试纸变蓝的原因:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.能使甲基橙变红的溶液中:Na+、NH4+、SO42-、NO3-
B.c(NO3-)=1mol/L的溶液中:H+、Fe2+、SO42-、Cl-
C.中性溶液中:NH4+、Fe3+、SO42-、Cl-
D.![]() =1×1012的溶液中:K+、Na+、S2O32-、F-
=1×1012的溶液中:K+、Na+、S2O32-、F-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:

名称 | 苯 | 溴 | 溴苯 |
密度/(g·cm-3) | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了________气体。继续滴加至液溴滴完。装置d的作用是___________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是___________________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是____________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必须用到的是________(填字母序号)。
a.重结晶b.过滤c.蒸馏d.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氟的卤素互化物通常作氟化剂,使金属氧化物转化为氟化物,如2Co3O4+6C1F3= 6CoF3+3C12+4X。下列有关该反应的说法,正确的是
A. X与O3互为同位素 B. ClF3中氯元素为-3价
C. Co3O4在反应中作氧化剂 D. lmol Co3O4参加反应转移9 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学分析中,常常需要用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配制准确物质的量浓度的KMnO4溶液。用Na2C2O4固体测定KMnO4溶液浓度的实验步骤如下:(反应原理为:5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O)
步骤一:先粗配浓度约为0.15mol/L的KMnO4溶液500mL。
步骤二:准确称取Na2C2O4固体mg放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配KMnO4溶液进行滴定。记录相关数据。
步骤三:重复步骤二两到三次。计算得KMnO4溶液的物质的量浓度。
试回答下列问题:
(1)盛放KMnO4溶液的滴定管为___(填“酸式”或“碱式”)滴定管。
(2)该滴定实验滴定终点的现象是___。
(3)步骤二中滴定操作如图所示,正确的操作是___(填编号)。
A. B.
B. C.
C.
(4)若m的数值为1.340g,滴定的KMnO4溶液平均用量为25.00mL,则KMnO4溶液的浓度为___mol/L。
(5)若滴定完毕后读数时俯视,则实验误差会__(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com