
ЁОЬтФПЁПXЁЂYЁЂZЁЂWЁЂRЪєгкжмЦкБэжаЧА20КХжїзхдЊЫиЃЌЧвдзгађЪ§вРДЮдіДѓЁЃдЊЫиXЕФЕЅжЪЪЧПеЦјжаЬхЛ§ЗжЪ§зюДѓЕФЦјЬхЃЌZЪЧдЊЫижмЦкБэжаЗЧН№ЪєадзюЧПЕФдЊЫиЃЌZКЭWЪЧЭЌзхдЊЫиЃЌRЕФзюЭтВуЕчзгЪ§ЪЧзюФкВуЕчзгЪ§ЕФвЛАыЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
A.дЊЫиXКЭYаЮГЩЕФЛЏКЯЮяОљЮЊЮоЩЋЦјЬх
B.дЊЫиZЁЂWЕФзюИпе§МлОљЮЊЃЋ7Мл
C.XЕФЧтЛЏЮягыWЕФЧтЛЏЮяЯргіЛсЩњГЩАзбЬ
D.ЛЏКЯЮяR2Y2жабєРызгКЭвѕРызгБШР§ЮЊ1ЁУ1
ЁОД№АИЁПC
ЁОНтЮіЁП
дЊЫиXЕФЕЅжЪЪЧПеЦјжаЬхЛ§ЗжЪ§зюДѓЕФЦјЬхЃЌXЪЧNдЊЫиЃЛZЪЧдЊЫижмЦкБэжаЗЧН№ЪєадзюЧПЕФдЊЫиЃЌZЪЧFдЊЫиЃЛZКЭWЪЧЭЌзхдЊЫиЃЌWЪЧClдЊЫиЃЛRЕФзюЭтВуЕчзгЪ§ЪЧзюФкВуЕчзгЪ§ЕФвЛАыЃЌRЪЧKдЊЫиЃЛXЁЂYЁЂZЁЂWЁЂRдзгађЪ§вРДЮдіДѓЃЌЫљвдYЪЧOдЊЫиЁЃ
A. дЊЫиNКЭOаЮГЩЕФЛЏКЯЮяжаЃЌNO2ЮЊКьзиЩЋЦјЬхЃЌЙЪAДэЮѓЃЛ
B. FдЊЫиУЛгае§МлЃЌЙЪBДэЮѓЃЛ
C. NH3гыHClЯргіЛсЩњГЩАзбЬNH4ClЃЌЙЪCе§ШЗЃЛ
D. ЛЏКЯЮяK2O2жаЕФвѕРызгЪЧ![]() ЃЌбєРызгКЭвѕРызгБШР§ЮЊ2ЁУ1ЃЌЙЪDДэЮѓЃЛ
ЃЌбєРызгКЭвѕРызгБШР§ЮЊ2ЁУ1ЃЌЙЪDДэЮѓЃЛ


 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПCOЁЂCO2ЪЧЛЏЪЏШМСЯШМЩеКѓЕФжївЊВњЮяЁЃ
ЃЈ1ЃЉЦћГЕХХЦјЙмФкАВзАЕФДпЛЏзЊЛЏЦїЃЌПЩЪЙЦћГЕЮВЦјжаЕФжївЊЮлШОЮязЊЛЏЮЊЮоЖОЕФДѓЦјбЛЗЮяжЪЁЃвбжЊЃКN2(g)ЃЋO2(g)===2NO(g)ІЄH=ЃЋ180.5kJЁЄmolЃ1
2C(s)ЃЋO2(g)===2CO(g)ІЄH=Ѓ221.0kJЁЄmolЃ1
C(s)ЃЋO2(g)===CO2(g)ІЄH=Ѓ393.5kJЁЄmolЃ1
дђЗДгІ2NO(g)ЃЋ2CO(g)===N2(g)ЃЋ2CO2(g)ЕФІЄH=________kJЁЄmolЃ1ЁЃ
ЃЈ2ЃЉвбжЊЃКЗДгІCO2(g)![]() CO(g)+O(g)дкУмБеШнЦїжаCO2ЗжНтЪЕбщЕФНсЙћШчЭМ1ЃЛЗДгІ2CO2(g)
CO(g)+O(g)дкУмБеШнЦїжаCO2ЗжНтЪЕбщЕФНсЙћШчЭМ1ЃЛЗДгІ2CO2(g)![]() 2CO(g)+O2(g)жа1molCO2дкВЛЭЌЮТЖШЯТЕФЦНКтЗжНтСПШчЭМ2ЃЌ
2CO(g)+O2(g)жа1molCO2дкВЛЭЌЮТЖШЯТЕФЦНКтЗжНтСПШчЭМ2ЃЌ
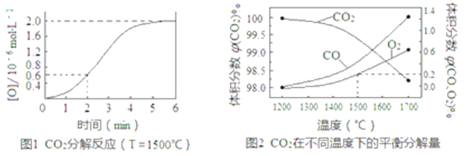
ЂйЗжЮіЭМ1ЃЌЧѓ2minФкv(CO2)=_______ЃЌ5minЪБДяЕНЦНКтЃЌЦНКтЪБcЃЈCOЃЉ=_______ЁЃ
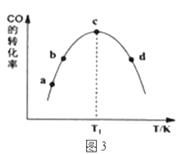
ЂкЗжЮіЭМ2ЃЌ1500ЁцЪБЗДгІДяЦНКтЃЌДЫЪБШнЦїЬхЛ§ЮЊ1LЃЌдђЗДгІЕФЦНКтГЃЪ§K=______(МЦЫуНсЙћБЃСє1ЮЛаЁЪ§)ЁЃ
ЃЈ3ЃЉЮЊЬНОПВЛЭЌДпЛЏМСЖдCOКЭH2КЯГЩCH3OHЕФбЁдёадаЇЙћЃЌФГЪЕбщЪвПижЦCOКЭH2ЕФГѕЪМЭЖСЯБШЮЊ1ЃК3НјааЪЕбщЃЌЕУЕНШчЯТЪ§ОнЃК
бЁЯю | T/K | ЪБМф/min | ДпЛЏМСжжРр | МзДМЕФКЌСП(%) |
A | 450 | 10 | CuO-ZnO | 78 |
B | 450 | 10 | CuO-ZnO-ZrO2 | 88 |
C | 450 | 10 | ZnO-ZrO2 | 46 |
ЂйгЩБэ1ПЩжЊЃЌИУЗДгІЕФзюМбДпЛЏМСЮЊ____________ЃЈЬюБрКХЃЉЃЛЭМ3жаaЁЂbЁЂcЁЂdЫФЕуЪЧИУЮТЖШЯТCOЕФЦНКтзЊЛЏТЪЕФЪЧ____________ЁЃ
ЂкгаРћгкЬсИпCOзЊЛЏЮЊCH3OHЕФЦНКтзЊЛЏТЪЕФДыЪЉга____________ЁЃ
AЃЎЪЙгУДпЛЏМСCuOЃZnOЃZrO2BЃЎЪЪЕБНЕЕЭЗДгІЮТЖШ
CЃЎдіДѓCOКЭH2ЕФГѕЪМЭЖСЯБШDЃЎКуШнЯТЃЌдйГфШыamolCOКЭ3amolH2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкУмБеШнЦїжаЕФвЛЖЈСПЛьКЯЦјЬхЗЂЩњЗДгІЃК![]() ЦНКтЪБВтЕУAЕФХЈЖШЮЊ0.50mol/L,БЃГжЮТЖШВЛБфЃЌНЋШнЦїЕФШнЛ§РЉДѓЕНдРДЕФСНБЖЃЌдйДяЦНКтЪБ,ВтЕУAЕФХЈЖШЮЊ0.30mol/LЁЃЯТСагаЙиХаЖЯе§ШЗЕФЪЧ
ЦНКтЪБВтЕУAЕФХЈЖШЮЊ0.50mol/L,БЃГжЮТЖШВЛБфЃЌНЋШнЦїЕФШнЛ§РЉДѓЕНдРДЕФСНБЖЃЌдйДяЦНКтЪБ,ВтЕУAЕФХЈЖШЮЊ0.30mol/LЁЃЯТСагаЙиХаЖЯе§ШЗЕФЪЧ
A.x+yЉzB.ЦНКтЯђе§ЗДгІЗНЯђвЦЖЏ
C.BЕФзЊЛЏТЪНЕЕЭD.CЕФЬхЛ§ЗжЪ§Щ§Ип
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЮяжЪжЎМфгаШчЯТЗДгІЙиЯЕЃК
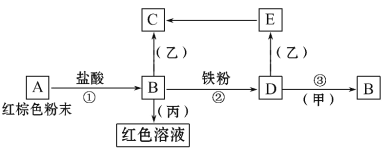
вбжЊгЩEзЊЛЏГЩCЕФЯжЯѓЪЧЃКАзЩЋГСЕэбИЫйБфЮЊЛвТЬЩЋЃЌзюКѓБфЮЊКьКжЩЋЁЃЛиД№ЃК
ЃЈ1ЃЉаДГіЯТСаЮяжЪЕФЛЏбЇЪНЃКA___ЃЌD___ЃЌМз___ЃЌБћ___ЁЃ
ЃЈ2ЃЉаДГіКьзиЩЋЗлФЉЕФвЛжжгУЭО___ЁЃ
ЃЈ3ЃЉаДГіEЁњCЗДгІЕФЛЏбЇЗНГЬЪН___ЁЃ
ЃЈ4ЃЉНЋБЅКЭЕФBШмвКЕЮШыЗаЫЎжаЫљЕУЗжЩЂЯЕжаЗжЩЂжЪПХСЃжБОЖЗЖЮЇЮЊ___ЁЃ
ЃЈ5ЃЉаДГіЗДгІЂкЕФРызгЗНГЬЪН___ЃЌИУЗДгІжаЃЌШчЙћга5.6gЬњЗлЭъШЋЗДгІдђЩњГЩDЕФЮяжЪЕФСПЮЊ___molЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГаЫШЄаЁзщРћгУЗЯЭаМЃЈКЌЭЁЂТСЕШЃЉжЦБИCuSO4ЁЄ5H2OОЇЬхЃЌжЦБИСїГЬШчЭМЃК
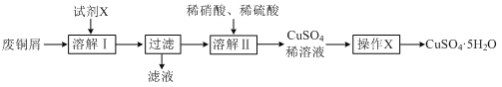
ЃЈ1ЃЉЁАШмНтЂёЁБЙ§ГЬжаЫљгУЪдМСXЮЊ___ЁЃЃЈЬюаДЪдМСУћГЦЃЉ
ЃЈ2ЃЉЁАШмНтЂђЁБЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ___ЁЃ
ЃЈ3ЃЉЁАВйзїXЁБАќРЈ___ЁЂЙ§ТЫЁЂЮоЫЎввДМЯДЕгЁЂЕЭЮТИЩдяЁЃ
ЃЈ4ЃЉФГжжЩБОњМСжаКЌCuSO4КЭCu(OH)2ЃЌЮЊВтЖЈЦфзщГЩЃЌаЫШЄаЁзщЩшМЦШчЯТЪЕбщЃКШЁвЛЖЈСПЕФЩБОњМСЃЌНЋЦфШмгкзуСПЕФЯЁбЮЫсжаЃЌШЛКѓЯђЦфжаМгШызуСПЕФBaCl2ШмвКЃЌЙ§ТЫИЩдяКѓЕУАзЩЋЙЬЬх2.33gЁЃШЛКѓЯђТЫвКжаЕЮМг1.00molЁЄL-1ЕФNa2H2Y(EDTA)ШмвКЃЌЗДгІжСжеЕуЪБЯћКФNa2H2YШмвК30.00 mL(РызгЗНГЬЪНЮЊCu2+ЃЋH2Y2-=CuY2-ЃЋ2H+)ЁЃ
ЂйгЩзМШЗГЦСПКѓЕФEDTAЙЬЬхХфжЦ100mL1.00molЁЄL-1ЕФEDTAШмвКЫљашЕФВЃСЇвЧЦїГ§ЩеБЁЂНКЭЗЕЮЙмЭтЛЙга___ЁЃ
ЂкЭЈЙ§МЦЫуШЗЖЈЩБОњМСжаCuSO4КЭCu(OH)2ЕФЮяжЪЕФСПжЎБШ___ЃЈаДГіМЦЫуЙ§ГЬЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкгаЛњЮяЕФЫЕЗЈе§ШЗЕФЪЧ
A.CH3CH(CH3)CH2CH2OHУћГЦЮЊЃК3ЃМзЛљЖЁДМ
B.![]() вЛТШДњЮяга5жж
вЛТШДњЮяга5жж
C.БъзМзДПіЯТЃЌ22.4LБћЯЉжаКЌга7NAИіІвМќЃЌNAИіІаМќ
D. ФмЗЂЩњЯћШЅЗДгІЃЌЦфВњЮяга2жж
ФмЗЂЩњЯћШЅЗДгІЃЌЦфВњЮяга2жж
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮЊЗРжЮЮэіВЃЌЩшМЦШчЯТСїГЬЮќЪеЙЄвЕЮВЦјSO2КЭNOЃЌЭЌЪБЛёЕУСЌЖўбЧСђЫсФЦ(Na2S2O4ЃЌЦфНсОЇЫЎКЯЮягжГЦБЃЯеЗл)КЭNH4NO3ВњЦЗЃЌвдБфЁАЗЯЁБЮЊБІЁЃ
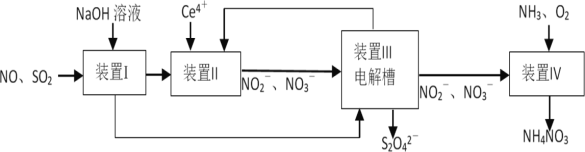
ЯТСаЫЕЗЈДэЮѓЕФЪЧ
A.S2O![]() жаМШДцдкЗЧМЋадМќгжДцдкМЋадМќ
жаМШДцдкЗЧМЋадМќгжДцдкМЋадМќ
B.зАжУIЕФзїгУЪЧЮќЪеSO2ЃЌзАжУIIЕФзїгУЪЧЮќЪеNO
C.БЃЯеЗлПЩЭЈЙ§зАжУЂѓжабєМЋВњЮяжЦБИЃЌCe4ЃЋДгвѕМЋПкСїГіЛиЕНзАжУIIбЛЗЪЙгУ
D.бѕЛЏзАжУIVжа1L 2molLЃ1NO![]() ЃЌжСЩйашвЊБъзМзДПіЯТ22.4LO2
ЃЌжСЩйашвЊБъзМзДПіЯТ22.4LO2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбаОПадбЇЯАаЁзщЭЌбЇЮЊСЫЬНОПЁАдкЯрЭЌЕФЮТЖШКЭбЙЧПЯТЃЌЯрЭЌЬхЛ§ЕФШЮКЮЦјЬхЖМКЌгаЯрЭЌЪ§ФПЕФЗжзгЁБЃЌЫћУЧвдНЬВФжаЯрЙиЃЈПЦбЇЬНОПЃЉЮЊЛљДЁЃЌЩшМЦСЫШчЭМЪЕбщзАжУВЂМЧТМЯрЙиЪЕбщЪ§ОнЁЃ
ЃЈЪЕбщзАжУЃЉ
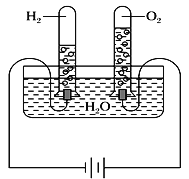
ЃЈВПЗжЪЕбщЪ§ОнЃЉ
ЮТЖШ | бЙЧП | ЪБМф | ЫЎВлжаH2OЕФжЪСП | H2ЬхЛ§ | O2ЬхЛ§ |
30 Ёц | 101 kPa | 0 | 300 g | 0 | 0 |
30 Ёц | 101 kPa | 4Зжжг | 298.2 g | 1.243 L |
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)4ЗжжгЪБH2ЁЂO2ЕФЮяжЪЕФСПЗжБ№ЪЧ________molЁЂ________molЁЃ
(2)ИУЮТЖШЯТЃЌЦјЬхФІЖћЬхЛ§ЪЧ__________ЁЃ
(3)дкИУЪЕбщЬѕМўЯТЃЌ3 mol O2ЕФЦјЬхЕФЬхЛ§ЮЊ____________L
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЃКЂйCH4ЃЈgЃЉ+2O2ЃЈgЃЉЈTCO2ЃЈgЃЉ+2H2OЃЈgЃЉЁїH1
ЂкCH4ЃЈgЃЉ+2O2ЃЈgЃЉЈTCO2ЃЈgЃЉ+2H2OЃЈlЃЉЁїH2
ЂлCH4ЃЈgЃЉ+![]() O2ЃЈgЃЉЈTCH3OHЃЈlЃЉЁїH3
O2ЃЈgЃЉЈTCH3OHЃЈlЃЉЁїH3
ЂмH2OЃЈgЃЉЈTH2OЃЈlЃЉЁїH4
ЂнCH3OHЃЈlЃЉ+![]() O2ЃЈgЃЉЈTCO2ЃЈgЃЉ+2H2OЃЈlЃЉЁїH5
O2ЃЈgЃЉЈTCO2ЃЈgЃЉ+2H2OЃЈlЃЉЁїH5
ЯТСаЙигкЩЯЪіЗДгІьЪБфЕФХаЖЯВЛе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
A.ЁїH1ЃОЁїH2B.ЁїH2=ЁїH1+ЁїH4C.ЁїH3=ЁїH2ЉЁїH5D.ЁїH4ЃМ0
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com