
【题目】某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+和Fe3+中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验:
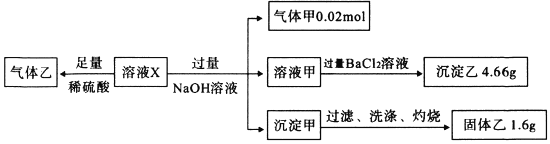
已知:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O则下列说法正确的是
A. 若含有Fe3+,则一定含有Cl-
B. SO42-、NH4+一定存在,Fe2+和Fe3+可能都存在
C. 该溶液中只存在上述离子中的NO3-、SO42-、NH4+、Fe2+四种离子
D. 气体甲能使湿润的蓝色石蕊试纸变红
【答案】C
【解析】某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+和Fe3+中的几种,且所含阴离子的物质的量相等,向溶液X中加过量的硫酸,有气体乙产生,发生的反应可能是CO32-与H+的反应,也可能是NO3-在H+条件下与Fe2+的氧化还原反应;溶液X与过量的NaOH溶液反应生成气体甲NH3为0.02mol,即溶液X中含0.02mol NH4+;所得的溶液甲中加氯化钡溶液,生成沉淀乙,则乙为BaSO4,质量为4.66g,则物质的量为0.02mol,即溶液X中含0.02mol SO42-;所得沉淀甲应为氢氧化亚铁或氢氧化铁或两者均有,经过滤、洗涤灼烧后所得的固体乙为Fe2O3,质量为1.6g,物质的量为0.01mol,故溶液X中含Fe2+或Fe3+或两者均有,且物质的量一定为0.02mol,由于Fe2+或Fe3+均能与CO32-发生双水解而不能共存,故溶液中无CO32-,则生成气体乙的反应只能是NO3-与Fe2+的氧化还原反应,故溶液中一定含Fe2+和NO3-,而所含阴离子的物质的量相等,即NO3-的物质的量也为0.02mol。故现在溶液X中已经确定存在的离子是:阴离子:0.02mol NO3-、0.02mol SO42-,共带0.06mol负电荷;阳离子:0.02mol NH4+,0.02molFe2+或Fe2+、Fe3+的混合物,所带的正电荷≥0.06mol,一定不含CO32-。根据溶液呈电中性可知,当 0.02mol全部是Fe2+时,阳离子所带正电荷为0.06mol,则氯离子一定不存在;若溶液中含Fe3+,阳离子所带正电荷大于0.06mol,则溶液中一定存在Cl-,A、由于溶液要保持电中性,故当溶液中含Fe3+时,则阳离子所带的正电荷>0.06mol,故溶液中一定含Cl-,A正确;B、SO42-、NH4+一定存在,Fe2+和Fe3+可能都存在,B正确;C、根据以上分析可知C错误;D、气体甲为氨气,能使湿润的蓝色石蕊试纸变红,D正确,答案选C。


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】已知N2和H2合成氨的反应是放热反应,破坏1mol N≡N键消耗的能量为Q1kJ,破坏1mol H-H键消耗的能量为Q2kJ,形成1mol N-H键放出的能量为Q3kJ,下列关系式中正确的是( )
A. Q1+3Q2>6Q3 B. Q1+3Q2<6Q3 C. Q1+Q2<Q3 D. Q1+Q2=Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关测定硫酸铜晶体中结晶水含量的实验中,使结果偏大的是
A.硫酸铜晶体中混有受热不分解的杂质
B.实验前被测样品已有部分失水
C.固体冷却时未放在干燥器中
D.加热时间过长,晶体略有发黑现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.25 L NaOH溶液中溶有10 g NaOH,则此溶液的物质的量浓度为( )
A.2 mo1/LB.1 mo1/LC.0.5 mo1/LD.0.05 mo1/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为
A. 盐酸、空气、硫酸、氨
B. 蒸馏水、氨水、碳酸氢钠、二氧化硫
C. 胆矾、盐酸、石墨、碳酸钙
D. 生石灰、水煤气、氯化铜、碳酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是电化学中的基本装置图,请根据条件回答问题
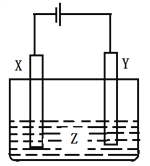
(1)若X为Cu、Y为石墨、Z为AgNO3溶液,则Y电极反应式为:________________________总反应为:______________________________
(2)若X为石墨、Y为Cu、Z为AgNO3溶液,则Y电极反应式为:________________________,总反应为:______________________________
(3)若要利用该装置实现“铜上镀银”,则X电极材料为:________,Y电极材料为:________,Z的溶液为:__________溶液
(4)若要利用该装置实现“精炼铜”的目的,则 Y极材料为:_______________.
(5)若要利用该装置实现“铁的防腐”,则铁应置于______位置。(填“X极”或“Y极”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用盐酸作标准液滴定待测浓度的NaOH溶液,若用酚酞指示剂,当滴定达终点时,溶液颜色变化是( )
A.由浅红色变无色B.由无色变浅红色C.由黄色变橙色D.由橙色变黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将浓度为2c mol·L-1、质量分数为a%的氨水,加水稀释至浓度为c mol·L-1,质量分数变为b%。则a、b之间的大小关系为 ( 已知:氨水的浓度越大密度越小 )
A. a=2b B. 2b>a>b C. a>2b D. 不能比较
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com