
【题目】普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型)。下列关于普伐他汀的描述正确的是( )
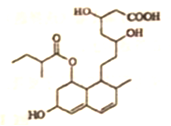
A. 分子中含有3种官能团
B. 可发生加成反应、氧化反应
C. 在水溶液中羧基和羟基均能电离出H+
D. 1mol该物质最多可与1molNaOH反应
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】现有三个体积相等的密闭容器中都进行如下反应:
CO2(g)+H2 (g)![]() CO(g)+H2O(g),反应所处的温度相同,但反应的起始浓度不同,其中甲:[H2]=[CO2]=amol 乙:[CO2]=amol [H2]=2amol 丙[CO2]=[H2]=[H2O]=amol,达到平衡时,CO的浓度由大到小的顺序排列正确的是
CO(g)+H2O(g),反应所处的温度相同,但反应的起始浓度不同,其中甲:[H2]=[CO2]=amol 乙:[CO2]=amol [H2]=2amol 丙[CO2]=[H2]=[H2O]=amol,达到平衡时,CO的浓度由大到小的顺序排列正确的是
A、丙>甲>乙 B、甲>乙>丙 C、乙>丙>甲 D、乙>甲>丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SnCl4是一种重要的工业原料,常作媒染剂等。已知SnCl4常温下是无色液体,在潮湿空气中易水解,熔点-36℃,沸点114℃。工业上制备SnCl4的工艺流程如下:

请回答下列问题:
(1)粗锡电解精炼时,常用硅氟酸(化学式为H2SiF6)和硅氟酸亚锡(化学式为SnSiF6)为电解液。已知H2SiF6为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为______。硅氟酸有腐蚀性,能与SiO2反应。电解时可选取下列电解槽中的________。
a.玻璃电解槽 b.不锈钢电解槽 c.塑料电解槽
阴极发生的电极反应式为_________。
(2)某同学模拟工业制法设计了由Sn与Cl2反应制取SnCl4的实验装置如下:

①a中浓盐酸与烧瓶内固体反应生成Cl2,则烧瓶内固体可以选用_________;仪器b的名称为_________。
②装置D的主要缺点是___________;除此之外,整套装置还有的缺点是_______。
③SnCl4溶液中加入适量的NaOH溶液,产生白色沉淀(二元酸),再加过量的NaOH溶液,白色沉淀溶解。试写出反应生成白色沉淀的离子方程式_________。
④若实验中取用锡粉5.95 g,反应后,E中广口瓶里收集到12.0 g SnCl4。则SnCl4的产率为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 用直接加热并蒸干FeCl3溶液的方法可制得纯净的无水FeCl3
B. 等物质的量浓度的Na2CO3溶液和CH3COONa溶液的pH,前者大于后者
C. 中和等体积、等物质的量浓度的盐酸和醋酸溶液,消耗NaOH的物质的量不相等
D. 对于有气体参加的反应,增大气体反应物浓度,活化分子百分数增大,反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的用途不正确的是( )
A.小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂
B.氧化铝可以作优良的耐火材料
C.Fe2O3常用作红色油漆和涂料
D.硅是制造光导纤维的材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:CH3CHO(g)+aO2(g)=X+bH2O(l) ΔH ,X为下列何种物质时ΔH最小
A. CH3COOH(l) B. CH3COOH(g) C. CO(g) D. CO2(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备水煤气的化学方程式如下:C(s)+H2O(g)![]() CO(g)+H2(g), 己知lmol的C完全反应吸收QkJ的热量,下列叙述正确的是
CO(g)+H2(g), 己知lmol的C完全反应吸收QkJ的热量,下列叙述正确的是
A. 增加C的量可以加快反应速率
B. 若将2molC 和足量的水蒸气混合,总共吸收的热量可为2QkJ
C. 反应至4 min时到平衡,若生成0.12mol H2,则CO的反应速率为0.03 mol/(L·min )
D. 当反应吸收热量为5QkJ时,断裂10NAH-O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌﹣锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)![]() Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
A. 电池工作时,锌失去电子
B. 电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e﹣=Mn2O3(s)+2OH﹣(aq)
C. 电池工作时,电子由正极通过外电路流向负极
D. 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既可以鉴别乙烷和乙炔,又可以除去乙烷中含有的乙炔的方法是 ( )
A. 足量的溴的四氯化碳溶液 B. 与足量的液溴反应
C. 点燃 D. 在一定条件下与氢气加成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com