
【题目】控制适合的条件,KI溶液过量,将反应2Fe3++2I-![]() 2Fe2++I2设计成如下图所示的原电池。下列判断正确的是( )
2Fe2++I2设计成如下图所示的原电池。下列判断正确的是( )
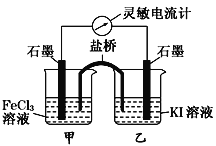
A. 反应开始时,甲中石墨电极为负极,发生氧化反应
B. 反应开始时,乙中石墨电极的反应式:I2+2e- = 2I-
C. 电流计读数为零时,在甲中加入KSCN溶液,出现血红色
D. 电流计读数为零时,反应处在停止状态
科目:高中化学 来源: 题型:
【题目】下列离子方程式错误的是( )
A. 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO![]() ===BaSO4↓+2H2O
===BaSO4↓+2H2O
B. 酸性介质中KMnO4氧化H2O2:2MnO![]() +5H2O2+6H+===2Mn2++5O2↑+8H2O
+5H2O2+6H+===2Mn2++5O2↑+8H2O
C. 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-===Mg(OH)2↓
D. 铅酸蓄电池充电时的阳极反应:PbSO4+2H2O-2e-===PbO2+4H++SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂废水中含有5.00×10-3mol/L的Cr2O72-,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4的流程图示意如下:

下列有关判断错误的是
A. 操作①中反应的离子方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
B. 操作②所得的滤渣成分主要为Fe(OH)3、Fe(OH)2、Cr(OH)3
C. 磁性材料Cr0.5Fe1.5FeO4中,显+3价铁与显+2价铁的质量之比为2∶3
D. 若废水中杂质不与绿矾反应,将该1 L废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4,理论上需加入绿矾13.9 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列有关说法错误的是( )
A.氮气化学性质不活泼,可用作食品防腐剂
B.石英是良好的半导体材料,可以制成光电池,将光能直接转化成电能
C.疫苗一般应冷藏存放,以避免蛋白质变性
D.家庭装修时用水性漆替代传统的油性漆,有利于健康及环境
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某种有机物分子的球棍模型图,图中的“棍”代表单键或双键,不同大小的“球”代表不同的短周期元素的原子,对该有机物的叙述不正确的是( ) 
A.该有机物可能的分子式为C2HCl3
B.该有机物可以由乙炔和氯化氢加成反应得到
C.该有机物分子中的所有原子在一个平面上
D.该有机物分子中一定有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属Na的叙述中,说法正确的是
A. Na在空气中燃烧,发出耀眼的白光
B. 金属钠可从氯化铁溶液中将铁置换出来
C. Na是银白色金属,密度小,硬度大,熔点高
D. 钠投入水中立即熔化成闪亮的小球,说明钠的熔点低,且钠与水反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,但使用过量会使人中毒。某学习小组针对亚硝酸钠设计了如下实验:
【实验Ⅰ】制取NaNO2
该小组先查阅资料知:①2NO+Na2O2 →2NaNO2;2NO2+Na2O2 →2NaNO3;②NO能被酸性高锰酸钾氧化为NO3-,然后设计制取装置如下图(夹持装置略去):

(1)装置A中用于盛放稀HNO3溶液的仪器名称为________;写出装置A中发生主要反应的离子方程式:__________。
(2)装置D的作用是____________;
(3)如果没有B装置,C中发生的副反应的化学方程式①_______ 、②______。
(4)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。下列哪种方案可以提高NaNO2纯度________。
A.将B中的药品换为碱石灰 B.将稀硝酸换为浓硝酸
C.实验开始前通一段时间CO2 D.在A、B之间增加盛有水的洗气瓶
【实验Ⅱ】测定NaNO2样品中NaNO3的含量
步骤:(1)配置KMnO4标准溶液并酸化,酸化KMnO4的酸应选择________(填化学式)
(2)已知在酸性溶液中,NO2-可将MnO4-还原为Mn2+。为测定亚硝酸钠的含量,称取4.000 g样品溶于水配成250 mL溶液,取25.00 mL溶液于锥形瓶中,用0.1000 mol·L-1酸性KMnO4溶液进行滴定,消耗KMnO4 20.00mL,酸性KMnO4的作用是______和_______,计算所得固体中亚硝酸钠的质量分数__________。(结果保留一位小数)
【扩展实验Ⅲ】该学习小组为再了解氧族元素的一些典型化合物的性质,进行了如下实验探究。
经查知:硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分 可能是SO2、SO3和O2中的一种、两种或三种。他们通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验用到的仪器如图所示:

(1)提出猜想
①所得气体的成分可能只含________一种;
②所得气体的成分可能含有________两种;
③所得气体的成分可能含有SO2、SO3和O2三种。
(2)实验探究
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。
请回答下列问题:
①请你组装探究实验的装置,按从左至右的方向,则仪器接口的连接顺序为______ (填序号)。
②由于加热时的温度不同,实验结束后测得相关数据也不同。数据如下:
实验 | 称取CuSO4的质量/g | 仪器C 增加的质量/g | 量筒中水的体积折算成标准状况下气体的体积/mL |
第一组 | 6.4 | 2.88 | 224 |
第二组 | 6.4 | 2.56 | 448 |
请通过计算,推断出第一组和第二组的实验条件下CuSO4分解反应的化学方程式:
第一组_________________; 第二组_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com