
【题目】化学与生产、生活密切相关。下列有关说法错误的是( )
A.氮气化学性质不活泼,可用作食品防腐剂
B.石英是良好的半导体材料,可以制成光电池,将光能直接转化成电能
C.疫苗一般应冷藏存放,以避免蛋白质变性
D.家庭装修时用水性漆替代传统的油性漆,有利于健康及环境
科目:高中化学 来源: 题型:
【题目】镁及其合金广泛应用于航空航天、交通、电池等行业。
已知:CaO(s)+3C(s)=CaC2(s)+CO(g) △H= +464 kJ·mol-1
MgO(s)+ CaC2(s)=CaO(s)+ Mg(g)+2C(s) △H =+177.5 kJ·mol-1
(1)镁可以在二氧化碳中燃烧,写出化学反应方程式_____________________。
(2)写出MgO(s)与C(s)生成1 mol CO(g)和气态镁的热化学方程式:________________。
(3) 用电解法制取镁时,若原料氯化镁含有水时,在电解温度下,原料会形成Mg(OH)Cl,并发生电离反应:Mg(OH)Cl=Mg(OH)++Cl-。电解时在阴极表面会产生氧化镁钝化膜,此时阴极的反应式为________________。
(4)镁/间二硝基苯电池工作时镁转变为氢氧化镁,间二硝基苯则转变为间二苯胺。间二硝基苯、间二苯胺的结构简式和镁/间二硝基苯电池的装置如下:
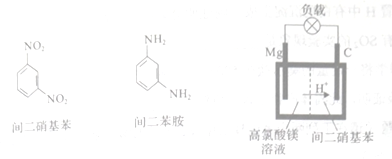
该电池放电时的正极反应方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是

A. 元素W的最高价氧化物对应水化物的酸性比Q的强
B. 原子半径的大小顺序为:r(W2-)>r(Q-)>r(Y2-)> r(Z3+)
C. 元素X与Q的氢化物化合的产物中既含共价键又含离子键
D. X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有c(CH3COOH)+c(CH3COO﹣)=0.1 molL﹣1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO﹣)与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述不正确的是( )

A. 由题给图示可求出25℃时醋酸的电离平衡常数Ka=10﹣4.75
B. W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH﹣)
C. pH=3.5的溶液中:c(Na+)+c(H+)﹣c(OH﹣)+c(CH3COOH)=0.1 molL﹣1
D. 向W点所表示的1.0 L溶液中通入0.05 molHCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH))+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方法中,不能用于实验室制取氨气的是( )
A.在烧瓶中将熟石灰和氯化铵混合,加水调成泥状后加热
B.加热试管中的氯化铵固体
C.将烧瓶中的浓氨水加热
D.将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制适合的条件,KI溶液过量,将反应2Fe3++2I-![]() 2Fe2++I2设计成如下图所示的原电池。下列判断正确的是( )
2Fe2++I2设计成如下图所示的原电池。下列判断正确的是( )
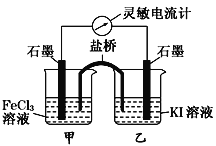
A. 反应开始时,甲中石墨电极为负极,发生氧化反应
B. 反应开始时,乙中石墨电极的反应式:I2+2e- = 2I-
C. 电流计读数为零时,在甲中加入KSCN溶液,出现血红色
D. 电流计读数为零时,反应处在停止状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”对化学反应提出了“原子经济性”(原子节约)的概念及要求。理想的原子经济性反应中原料分子中的所有原子全部转变成所需产物,不产生副产物,实现零排放。以下反应中符合“绿色化学”的是( )
A. 以苯和乙醇为原料,在一定条件下生产乙苯
B. 利用乙烷与氯气反应,制备氯乙烷
C. 乙烯与氧气在银的催化作用下生成环氧乙烷(结构简式如图)
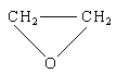
D. 乙醇与浓硫酸共热制备乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应Fe+H2SO4=FeSO4+H2↑,回答下列问题.
(1)在此反应中,自反应开始至2分钟末,H2SO4浓度由1mol/L变为0.4mol/L,则H2SO4的反应速率为 .
若要使该反应的反应速率加快,下列措施不可行的是(填字母)
a、改铁片为铁粉 b、改稀H2SO4为98%的浓H2SO4
c、升高温度 d、滴加少量CuSO4溶液
(2)在答题卡的坐标图中,画出此反应过程中体系的能量变化图(进行必要的标注)
(3)根据此反应设计一个原电池,要求画出装置图并进行必要的标注 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期.C、B可按原子个数比2:1和1:1分别形成两种离子化合物甲和乙.A原子的最外层电子数比次外层电子数多3个.E是地壳中含量最高的金属元素.根据以上信息回答下列问题:
(1)D元素在周期表中的位置是 , 中子数为14的E原子可表示为 .
(2)写出由A和C形成的化合物的化学式 , 该化合物由键形成.
(3)A、B、C、D、E五种元素的离子半径由小到大的顺序是(用离子符号填写).
(4)写出实验室制取A的气态氢化物的化学方程式: .
(5)简述比较D与E金属性强弱的实验方法: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com