
科目:高中化学 来源: 题型:
(1)下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
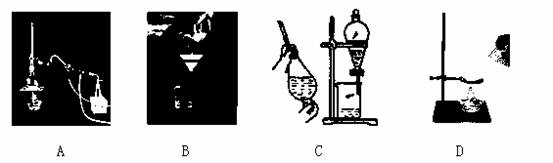
根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置(将A、B、C、D填入适当的空格中)。
①除去Ca(OH)2溶液中悬浮的CaCO3 ; ②从碘水中提取碘 ;
③用自来水制取蒸馏水 ; ④分离植物油和水 ;
⑤除去食盐水中的泥沙 ; ⑥与海水晒盐原理相符的是 。
(2)由可溶性铝盐制取氢氧化铝,需加入的试剂为: ;
离子方程式为: 。
白色的Fe(OH)2在空气中发生的颜色变化为 。
反应的化学方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物F是一种重要的有机合成中间体,它的合成路线如下:

(1)化合物F中含氧官能团的名称是 ▲ 和 ▲ ,
由B生成C的化学反应类型是 ▲ 。
(2)写出化合物C与乙酸反应生成酯的化学方程式: ▲ 。
(3)写出化合物B的结构简式: ▲ 。
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢。写出该化
合物的结构简式: ▲ (任写一种)。
(5)请根据已有知识并结合相关信息,写出以苯酚( )和CH2=CH2为原料制备
)和CH2=CH2为原料制备
 |
有机物 的合成路线流程图(无机试剂任用)。
|

|
|
 H2C== CH2
H2C== CH2 CH3CH2Br CH3CH2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.在相同条件下,若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由 “C(石墨)=C(金刚石);ΔH = +119kJ·mol-1 ”可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH—(aq)=H2O(l);ΔH = -57.3l kJ·mol-1,若将含0.5mol H2SO4的浓硫酸与lmol NaOH溶液混合,放出的热量大于57.31 kJ
D.在101KPa时,2g H2完全燃烧生成液态水,放出285.8 kJ 热量,氢气燃烧的热化学
方程式表示为:H2(g)+1/2O2(g)=H2O(l);ΔH = + 285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示为某些有机物之间的相互转化关系,其中A、B属于芳香族化合物,且B不能使FeCl3溶液显紫色,H是衡量一个国家石油化工发展水平标志的物质。
 |
请回答下列问题:
(1)C、D的相对分子质量之差是 ,G的结构简式是 。
(2)写出下列反应类型:① ;⑥ 。
(3)写出D中官能团的名称
(4)写出反应③、⑦的化学方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
氰氨基化钙是一种重要的化工原料,其制备的化学方程式为:CaCO3+2HCN = CaCN2+CO↑+H2↑+CO2↑,下列说法正确的是
A.CO为氧化产物,H2为还原产物 B.CaCN2中含有非极性键
C.HCN既是氧化剂又是还原剂 D.每消耗10g CaCO3生成2.24L CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
为了测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。
B.用某仪器量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。
C.将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。
D.将物质的量浓度为M mol/L的标准NaOH溶液装入碱式滴定管,调节液面记下开始读数为V1mL。
E.在锥形瓶下垫一张白纸,滴定至恰好反应为止,记下读数为V2mL。
F.把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G.用某仪器准确量取浓硫酸样品10.00 mL,在烧杯中用蒸馏水溶解。
就此实验操作完成下列填空:
(1)正确操作步骤的顺序(用编号字母填写) → A → → → → → 。
(2)用来量取10.00mL浓硫酸的仪器是 。
(3)滴定中可选用的指示剂是 ;滴定中,目光应注视 ;
判断滴定恰好完成的依据是 ;读数时,目光与凹液面的最低处保持水平。
(4)某学生实验时用稀硫酸润洗了锥形瓶,测定的浓度会 (填“偏高”、“偏低”或“不变”)。
(5)该浓硫酸样品浓度的计算式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com