
随着世界粮食需求量的增加,农业对化学肥料的需求越来越大。氮肥是需求最大的一种化肥。氮肥的生产和合理施用在农业生产中起着重大作用。合成氨及化肥生产流程示意图如下:
(1)目前,工业上用铁触媒作催化剂,在20~50 MPa、450℃左右用氮、氢混合气体在________中进行合成氨。则沿X方向回去的物质是________。
(2)目前生产尿素是以氨气与CO2为原料,发生反应的化学方程式是________、________。
尿素适用于各种土壤,在土壤中尿素发生水解,其水解的化学方程式是________。
(3)沉淀池中发生反应的化学方程式是________________。
(4)上述生产中的副产品氯化铵长期使用会造成土壤酸化、变硬甚至板结。对土壤的酸碱性进行测定与改良是保护________、提高土壤肥力的有效途径。测定土壤的pH的方法是________。
科目:高中化学 来源: 题型:单选题
下列说法中,不正确的是
| A.现代科学技术的发展和环境问题的解决离不开化学科学 |
| B.门捷列夫提出的元素周期律为发现新元素、合成新材料提供了新思路 |
| C.绿色化学最显著的特征是在生产化工产品过程中必须利用绿色植物为原料 |
| D.植物的光合作用是地球上规模最大的化学反应,在生物体内把光能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(15分)【化学——选修2:化学与技术】
(一)硫酸厂常用煅烧黄铁矿(FeS2)来制取硫酸。
(1)煅烧黄铁矿的主要化学方程式为 。
(2)SO2和O2的反应为 2SO2(g)+O2(g) 2SO3(g),该反应在体积不变的密闭容器中进行,则下列 (填序号)可作为反应达到平衡的判断依据。
2SO3(g),该反应在体积不变的密闭容器中进行,则下列 (填序号)可作为反应达到平衡的判断依据。
A.v正(SO2)=v正(SO3)
B.各组分的体积分数不再变化
C.反应体系的温度不再变化
D.混合气体的平均相对分子质量不再变化
E.混合气体的密度不再变化
(3)热交换器是实现冷热交换的装置,化学实验中也经常利用热交换来实现某种实验目的。试分析气、液热交换时通常使用的仪器是________________________。(写名称)
(4)硫酸工业所产生的尾气除了含有N2、O2外,还含有SO2,微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的试剂是___________________。(填序号)
A.NaOH溶液、酚酞试液 B.KMnO4溶液、稀硫酸
C. 氨水、酚酞试液 D.碘水、淀粉溶液
(二)实验室常用硫酸厂的烧渣(主要成分是Fe2O3及少量FeS、SiO2)来制备绿矾(FeSO4·7H2O)。
其中测定绿矾产品中FeSO4·7H2O含量的实验步骤为:
a.称取5.2 g产品,溶解,配成250 mL溶液
b.量取25.00 ml待测液于锥形瓶中
c.用硫酸酸化的0. 01 mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积35.00 mL。
据此,请分析:
(1)滴定时反应的离子方程式为(完成并配平离子反应方程式)。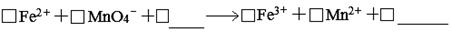
(2)滴定达到终点的标志是 。
(3)产品中FeSO4·7H2O的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
水是生命之源,也是重要的环境要素之一。
(1)观察下图(Ⅰ),若用1 L水来代表地球上的总水量,要比较精确地量取地球上的淡水量,应选择的仪器是__________。
| A.100 mL烧杯 | B.50 mL烧杯 | C.100 mL量筒 | D.50 mL量筒 |
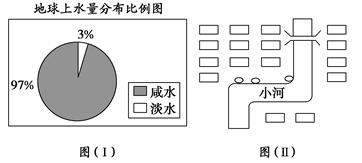

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
当前,大量施用氮素化肥是冬小麦获得高产的重要措施之一。
(1)施入土壤的氮素化肥主要以________形式被小麦根部吸收,透气性较好的土壤植物容易吸收氮素化肥,透气性较差的黏质土壤,则根的吸肥力差,这是因为_______________________________________________。
(2)施肥后要及时灌溉,若从麦田流失的水从下图A位置注入一条河流,导致下游水体中藻类和细菌数量发生的变化如下列曲线图所示:
①在A的下游藻类数量增加的原因是____________________________________________________________。
②在3 km以外的河段,细菌数量迅速增加的原因是_____________________________________________________________。
③在下游6 km处的河段发现鱼类大量死亡,原因是______________________________________________________________。
④在距A 2 km处,水中的氧气含量比A处高,原因是______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下(金属单质E可由滤液C制取):
已知:Cu2O + 2H+ =" Cu" + Cu2+ + H2O。
(1)滤液A中铁元素的可能存在形式为_______(填离子符号),与之相关的离子方程式为_____________,若滤液A中存在Fe3+,检验该离子的试剂为________(填试剂名称)。
(2)写出E和F反应生成铜的化学方程式为_____________________________。
(3)利用电解法进行粗铜精炼时,下列叙述正确的是_________(填代号)。
a.若用硫酸铜溶液作电解液,SO2- 4向阴极移动
b.粗铜接电源正极,发生还原反应
c.精铜作阴极,电解后电解液中Cu2+浓度减小
d.当粗铜消耗6.4 g时,转移0.2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
工业上以碳素铬铁为原料制取铬铵矾,利用电解法制取金属铬。其工艺流程如下图所示。
已知:FeSO4+Cr=CrSO4+H2↑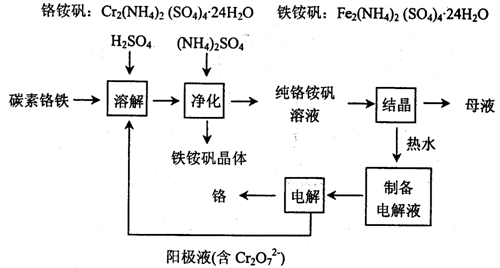
(1)碳素铬铁是铁铬合金,粉碎后溶于硫酸和电解阳极液的混合溶液中。该过程中电解阳极液的主要作用是 。
(2)加入(NH4)2SO4的目的是 。
(3)结晶后的母液从绿色化学的角度可采用的处理方法是 。
(4)产品铬中含氧呈脆性,为了降低其含氧量,可通过 提高其纯度。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有A、B、C、D四个中等城市,它们水源、能源充足,交通便利。它们相对地理位置如下图所示。各城市各有其特点:A城是风光秀丽,人口稠密,土地供应紧张的旅游城市,环保要求高,近郊有丰富的FeS2资源;B城是一个新兴的工业城市,已建有大型磷肥厂,土地供应充足。C城近郊有丰富的磷灰石资源,工业发达,但使用H2SO4的工业不多,土地供应充足;D城是一个古老的城市,它的周围是重要的农业区,是大量肥料的集散地。现拟建年产1×105 t硫酸的工厂,厂址应选在 ( )。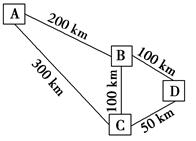
A.A城近郊 B.B城近郊 C.C城近郊 D.D城近郊
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com