
| A、①③ | B、①④ | C、②③ | D、③④ |
| ||
| 2s |
| ||
| 2s |
| 1.2mol |
| 4mol |
| 1.4mol |
| 2L |


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
| A、碱、纯碱、Na2CO3 |
| B、单质、氯水、Cl2 |
| C、酸、硫酸、H2S |
| D、酸性氧化物、干冰、CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
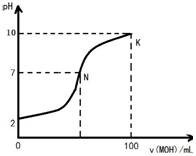 常温下,向100mL 0.01mol?L-1盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向100mL 0.01mol?L-1盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、MOH是弱碱 | ||
| B、N点c(Cl-)=c(M+) | ||
C、随着MOH溶液的滴加,比值
| ||
| D、K点对应的溶液c(MOH)+c(OH-)-c(H+)=0.001mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化铁胶体中分散质微粒直径为1-100nm |
| B、可利用渗析的原理提纯胶体 |
| C、可用丁达尔现象判断胶体的制备是否成功 |
| D、电泳现象说明了胶体带电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
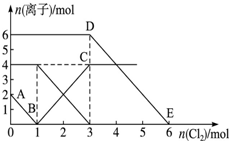 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.已知:Cl2+2Br-═2Cl-+Br2,2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.则下列说法中不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示.已知:Cl2+2Br-═2Cl-+Br2,2Fe2++Br2═2Fe3++2Br-,2Fe3++2I-═2Fe2++I2.则下列说法中不正确的是( )| A、还原性:I->Fe2+>Br- |
| B、原混合溶液中FeBr2的物质的量为3mol |
| C、线段AB表示Fe2+被氯气氧化 |
| D、原溶液中:n(Fe2+):n(I-):n(Br-)═2:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2、CS2、HI都是直线形的分子 |
| B、BF3键角为120°,SnBr2键角大于120° |
| C、COCl2、BF3、SO3都是平面三角形的分子 |
| D、PCl3、NH3、PCl5都是三角锥形的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.714g/mL |
| B、0.714g/L |
| C、0.179g/L |
| D、0.275g/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
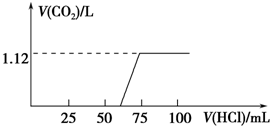 某化学兴趣小组同学用实验室中一瓶久置的NaOH固体做了以下实验:先称取13.3g NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入浓度为4mol?L-1的盐酸,再根据生成的CO2体积计算出Na2CO3质量,从而进一步计算出样品中变质NaOH的质量.实验测得加入盐酸的体积与产生CO2的体积(标况)关系如图所示:
某化学兴趣小组同学用实验室中一瓶久置的NaOH固体做了以下实验:先称取13.3g NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入浓度为4mol?L-1的盐酸,再根据生成的CO2体积计算出Na2CO3质量,从而进一步计算出样品中变质NaOH的质量.实验测得加入盐酸的体积与产生CO2的体积(标况)关系如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com