
 用如图所示的装置进行实验:
用如图所示的装置进行实验:

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
| A、能生成碱的金属元素都在ⅠA族 |
| B、稀有气体元素原子的最外层电子数均为8 |
| C、第二周期ⅣA族元素的原子核电荷数和种子数一定为6 |
| D、原子序数为14的元素位于元素周期表的第3周期ⅣA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
35 17 |
37 17 |
 与
与  ⑥CH3-CH2-OH和CH3-O-CH3
⑥CH3-CH2-OH和CH3-O-CH3查看答案和解析>>
科目:高中化学 来源: 题型:
| A、目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现 |
| B、元素的性质随着原子序数的增加而呈周期性变化 |
| C、俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 |
| D、最外层电子数为8的粒子是稀有气体元素的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
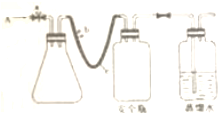 实验室用下列方法测定某水样中O2的含量
实验室用下列方法测定某水样中O2的含量2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、氯原子的结构示意图: | ||
B、H2O分子的比例模型: | ||
C、作为相对原子质量测定标准的碳核素:
| ||
D、用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com