
 ���������̬�⻯����ȶ���С�ڣ�����ڡ���С�ڡ���NH3��
���������̬�⻯����ȶ���С�ڣ�����ڡ���С�ڡ���NH3��
���� ��1��N��O�������ֱ�Ϊ��7��8�����ߵ�������֮����15��������15��PԪ�أ��ݴ˿ɻ����ṹʾ��ͼ������NԪ����ͬ���壬�ǽ����ԣ�P��N���ݴ��ж���̬�⻯����ȶ��ԣ�
��2��笠�����ˮ�������ԣ�
��3��������ƣ�������ơ������P���ᣩ��ˮ�ܽ⣬���˵ú�����ƺ��������Һ������̼��������ᷴӦ��������ơ�ˮ�Ͷ�����̼���壬��ͨ�백���к�������������泥��������õ���ҺΪ����ƺ�����淋Ļ����Һ�������ᾧ�õ�����笠�[5Ca��NO3��2•NH4NO3•10H2O]���壻
��4���ٸ���Ĥ��ⷨ������Ϊˮʧ���ӷ�����������Ӧ��������������������ʹ������ǿ�����������ƶ����������ϳ����
�ڵ��ʱ������Ϊ����ӦΪ�����ӵõ��ӷ�����ԭ��Ӧ������������ʹ������ǿ�����������ƶ���笠����ӷ�Ӧ���ɰ������ݴ˷�����
��� �⣺��1��N��O�������ֱ�Ϊ��7��8�����ߵ�������֮����15��������15��PԪ�أ���ԭ�ӵĽṹʾ��ͼΪ ������NԪ����ͬ���壬�ǽ����ԣ�P��N��������̬�⻯����ȶ��ԣ�PH3��NH3��
������NԪ����ͬ���壬�ǽ����ԣ�P��N��������̬�⻯����ȶ��ԣ�PH3��NH3��
�ʴ�Ϊ�� ��С�ڣ�
��С�ڣ�
��2��笠�����ˮ�������ԣ���ˮ�����ӷ�ӦΪNH4++H2O?NH3•H2O+H+��
�ʴ�Ϊ��NH4++H2O?NH3•H2O+H+��
��3���������Ϊ������ˮ�����ʣ�����������Ҫ�ɷ�������ƣ���ѧʽΪCa3��PO4��2��
�ʴ�Ϊ��Ca3��PO4��2��
�ڼ���̼��������ᷴӦ��������ơ�ˮ�Ͷ�����̼���壬������Ӧ�����ӷ���ʽΪCaCO3+2H+�TCa2++CO2��+H2O��
�ʴ�Ϊ��CaCO3+2H+�TCa2++CO2��+H2O��
�ۿ����к���������������ֱ��ǵ���������������������ԭ��Ӧԭ���ó�����立ֽⷽ��ʽΪ��2NH4NO3$\frac{\underline{\;230��400��\;}}{\;}$2N2��+O2��+4H2O��
�ʴ�Ϊ��2NH4NO3$\frac{\underline{\;230��400��\;}}{\;}$2N2��+O2��+4H2O��
��3����Ĥ��ⷨ������Ϊˮʧ���ӷ�����������Ӧ����ӦʽΪ2H2O-4e-�T4H++O2���������������������������ʹ������ǿ�����������ƶ����������ϳ����ᣬ���Ԣ��ҿɻ��յIJ�ƷΪ���
�ʴ�Ϊ��2H2O-4e-�T4H++O2�������
�ڵ��ʱ������Ϊ����ӦΪ�����ӵõ��ӷ�����ԭ��Ӧ����2H++2e-=H2����������������ʹ������ǿ�����������ƶ���笠����ӷ�Ӧ���ɰ�����������Ӧ��NH4++OH-=NH3+H2O�����Ԣ��ҿɻ��յ�������
�ʴ�Ϊ�����ʱ���������ӵõ��ӷ�����ԭ��Ӧ����2H++2e-=H2����ʹ������ǿ��ͬʱNH4+ͨ��������Ĥ����III �ң�������Ӧ��NH4++OH-=NH3+H2O�����ɰ�����
���� ������Ҫ�����˹�ҵ��������笠Ƶ�ԭ������ˮ�Ĵ��������ڿ��鿼���Ķ�����Ϣ����������������������װ�õķ�������缫��Ӧʽ����д���״��㣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �٢� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
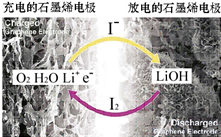 ��ѧ�ҿ�����һ�������-����أ��������ܶȼ��ߣ�Ч�ʴﵽ90%���ϣ���������ӵ⻯ﮣ�LiI������ˮ������ԭ����ͼ��ʾ���ܷ�ӦΪ��O2+4LiI+2H2O$?_{���}^{�ŵ�}$2I2+4LiOH���ڸõ�ص�����˵������ȷ���ǣ�������
��ѧ�ҿ�����һ�������-����أ��������ܶȼ��ߣ�Ч�ʴﵽ90%���ϣ���������ӵ⻯ﮣ�LiI������ˮ������ԭ����ͼ��ʾ���ܷ�ӦΪ��O2+4LiI+2H2O$?_{���}^{�ŵ�}$2I2+4LiOH���ڸõ�ص�����˵������ȷ���ǣ�������| A�� | ���ʱ������ӦΪLiOH+e-�TLi+OH | |
| B�� | ���ʱLi+������������������ | |
| C�� | �ŵ�ʱ������ӦΪO2+2H2O+4Li++4e-�T4LiOH | |
| D�� | �ŵ�ʱ������I- ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HA��Һ�м���NaA�����$\frac{c��HA��c��O{H}^{-}��}{c��{A}^{-}��}$��С | |
| B�� | �����£�0.1mol/LHA��Һ��ˮ�����c��H+��Ϊ10-13mol/L | |
| C�� | �����£�0.1mol/LNaA��Һˮ�ⳣ��Ϊ10-9 | |
| D�� | NaA��Һ�м���HCl��Һ��ǡ����ȫ��Ӧ�����ڹ�ϵ��2c��Na+���Tc��A-��+c��Cl-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | ֻ�Т� | D�� | ȫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
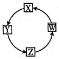 X��Y��Z��W�������ʼ��ת����ϵ��ͼ��ʾ������ת����ϵ�в���һ��ʵ�ֵ���
X��Y��Z��W�������ʼ��ת����ϵ��ͼ��ʾ������ת����ϵ�в���һ��ʵ�ֵ���| ѡ�� | X | Y | Z | W |
| A | Na | Na2O2 | NaOH | NaCl |
| B | H2S | SO2 | SO3 | H2SO4 |
| C | Fe | FeCl3 | Fe��OH��3 | Fe2O3 |
| D | AlCl3 | NaAlO2 | Al��OH��3 | Al |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼���ƣ�s�� | B�� | �����ƣ�s�� | C�� | �������ƣ�aq�� | D�� | ����أ�aq�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǰ�ߴ��ں��� | B�� | ǰ��С�ں��� | C�� | ��� | D�� | ����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ٺ͢� | B�� | �� | C�� | �ۺ͢� | D�� | ���϶����� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com