
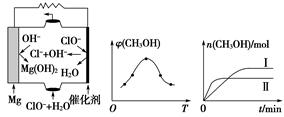
 CH3OH(g)+H2O(g) ΔH。
CH3OH(g)+H2O(g) ΔH。 +8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O
+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O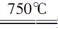 2MgO+SO2+CO2+SO3
2MgO+SO2+CO2+SO3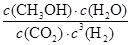 ②< ③>
②< ③>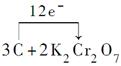 +8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。
+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4)3+8H2O。

科目:高中化学 来源:不详 题型:单选题
| A.Cu与Cu2O的物质的量之比为2∶1 |
| B.硝酸的物质的量浓度为2.6 mol·L-1 |
| C.产生的NO在标准状况下的体积为4.48 L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.电解时发生反应的化学方程式为2HCl Cl2↑+H2↑ Cl2↑+H2↑ |
| B.由NaClO2溶液制取0.6 mol ClO2时,至少消耗0.1 mol NCl3 |
| C.将产生的混合气体通过盛有碱石灰的干燥器以除去ClO2中的NH3 |
| D.溶液X的主要成分为NaClO2和NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Fe(OH)3+5OH-]
Fe(OH)3+5OH-]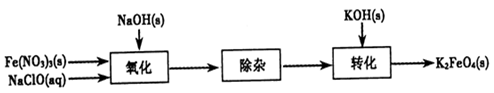
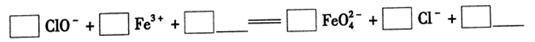
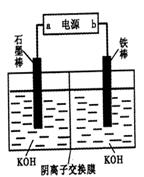
 4Fe(OH)3+8OH-+3O2。实验测得K2FeO4溶液浓度与温度和pH的关系分别如下图所示:
4Fe(OH)3+8OH-+3O2。实验测得K2FeO4溶液浓度与温度和pH的关系分别如下图所示: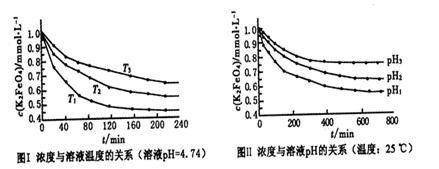
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学方程式中产物分子的化学计量数由小到大的顺序是SO2、N2、NH3、H2O |
| B.氧化产物和还原产物的物质的量之比为3∶1 |
| C.被氧化元素原子和被还原元素原子的物质的量之比为2∶3 |
| D.若反应生成1 mol H2O,则转移的电子为6 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

 +2FeS+SO2(已配平),则下列关于该反应的说法错误的是( )。
+2FeS+SO2(已配平),则下列关于该反应的说法错误的是( )。| A.方框中的物质应为CuS |
| B.该反应的部分产物可用于硫酸工业 |
| C.反应中SO2既是氧化产物又是还原产物 |
| D.反应中若有1 mol SO2生成,则一定有4 mol电子发生转移 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
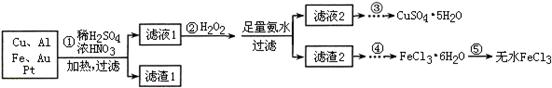
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液(mL) | 25.00 | 25.02 | 26.20 | 24.98 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Fe3O4+S4O62-+2H2O,有关说法正确的是
Fe3O4+S4O62-+2H2O,有关说法正确的是| A.每转移1.5mol电子,有1.125mol Fe2+被氧化 |
| B.x = 2 |
| C.Fe2+、S2O32-都是还原剂 |
| D.每生成1mol Fe3O4,转移电子2mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO(NH2)2 (l) + H2O (l)。
CO(NH2)2 (l) + H2O (l)。 ,右图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是___________。
,右图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com