
【题目】下列实验操作、现象与预期实验目的或所得实验结论一致的是

A.AB.BC.CD.D
【答案】A
【解析】
A. 等体积饱和溶液中,溶质溶解度大的反应产生的沉淀多;
B. 银镜反应需在碱性条件下进行;
C. SO2水溶液显酸性,溶液中含SO32-浓度很小,根据BaSO4不溶于水,也不溶于酸,而BaSO3不溶于水,但能溶于酸;
D. 先判断物质的过量问题,然后判断反应的可逆性。
A. AgCl、AgBr在溶液中存在沉淀溶解平衡,向等体积AgCl、AgBr饱和溶液中加入足量AgNO3浓溶液,产生沉淀的物质的量AgCl>AgBr,说明溶液中含有AgCl>AgBr,因此可证明物质的溶度积常数Ksp(AgCl)>Ksp(AgBr),A正确;
B. 向20%的蔗糖溶液中加入一定体积稀硫酸,加热,使蔗糖发生水解反应,然后加入NaOH中和硫酸,使溶液显碱性,然后再加入银氨溶液,水浴加热,才可以发生银镜反应,否则不能证明蔗糖是否发生水解反应,B错误;
C. 向BaCl2溶液中通入SO2气体和气体X,产生白色沉淀,该气体可能是碱性气体NH3,反应产生的白色沉淀是BaSO3;也可能是具有氧化性的气体如Cl2,反应产生的是BaSO4白色沉淀,C错误;
D. FeCl3与KI会发生反应:2FeCl3+2KI=2FeCl2+I2+2KCl,n(FeCl3)=5×10-4 mol>n(KI)=1×10-4 mol,FeCl3溶液过量,所以取反应后上层清液滴加KSCN溶液,溶液变为红色,不能证明该反应为可逆反应,D错误;
故合理选项是A。


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.向NaHCO3溶液中通入CO2至pH=7,则c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B.室温下,浓度均为0.1mol/L的CH3COOH、CH3COONa混合溶液的pH=4,则c(CH3COO-)-c(CH3COOH)=2×(10-4-10-10)mol/L
C.加水稀释0.1mol/L醋酸溶液,溶液中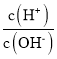 增大
增大
D.室温下,NaHA溶液的pH<7,则一定有c(Na+)=c(HA-)+c(H2A)+c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式_____________ ;
(2)用如图所示装置可检验木炭和浓硫酸反应产生的混合气体中含有SO2和CO2。
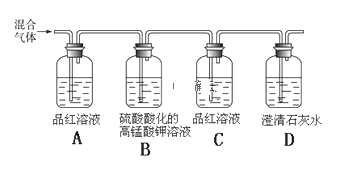
①能够证明混合气体中含有SO2的实验现象是:________________________________;
②设计B、C的实验目的是:________________________________________________;
③写出B中发生反应的离子方程式:_____________________________;
④能够证明混合气体中含有CO2的实验现象是:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用18.4molL-1的浓硫酸来配制480mL0.2molL-1的稀硫酸。可供选用的仪器有:①胶头滴管②烧瓶③烧杯④药匙⑤量筒⑥托盘天平⑦玻璃棒
请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有___(选填序号),还缺少的仪器有(写仪器名称)___。
(2)需要用量筒量取上述浓硫酸的体积为___mL,量取浓硫酸时应选用___(选填①10mL②50mL③100mL)规格的量筒。
(3)实验中两次用到玻璃棒,其作用分别是:___、___。
(4)下列对容量瓶及其使用方法的描述中正确的是___。
A.容量瓶上标有容积、温度和浓度
B.容量瓶用蒸馏水洗净后,必须烘干
C.配制溶液时,把量好的浓硫酸小心倒入容量瓶中,加入蒸馏水到接近刻度线1~2cm处,改用胶头滴管加蒸馏水至刻度线
D.使用前要检查容量瓶是否漏水
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有___(填序号)
①未洗涤稀释浓硫酸时用过的烧杯和玻璃棒
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Z是合成某药物的中间体,其合成原理如下:
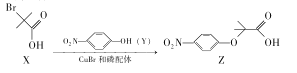
下列说法正确的是.
A.用NaHCO3溶液可以鉴别X和ZB.X、Y、Z都能发生取代反应
C.X分子所有碳原子可能共平面D.与X具有相同官能团的同分异构体还有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知磷酸分子(![]() )中的三个氢原子都可与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。则下列说法正确的是
)中的三个氢原子都可与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。则下列说法正确的是
A.H3PO2在水溶液中发生电离:H3PO2![]() H++H2PO2-、H2PO2-
H++H2PO2-、H2PO2-![]() H++HPO22-
H++HPO22-
B.H3PO4属于三元酸、H3PO2属于二元酸
C.NaH2PO2属于酸式盐,其水溶液呈酸性
D.H3PO2具有较强的还原性,其结构式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告中提出“打赢蓝天保卫战”,对污染防治要求更高。某种利用垃圾渗透液实现发电、环保二位一体结合的装置示意图如下。当该装置工作时,下列说法正确的是
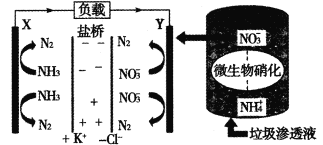
A.盐桥中Cl-向Y极移动
B.电路中流过7.5 mol电子时,共产生N2的体积为44.8 L(标况)
C.电流由X极沿导线流向Y极
D.Y极发生的反应为2NO3-+10e-+6H2O=N2↑+12OH-,周围pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁是一种特殊的金属有机化合物,可用作燃料的节能消烟剂、抗爆剂等,熔点为173 ℃,在100 ℃时开始升华;沸点是249 ℃。实验室制备二茂铁的反应原理是:2KOH+FeCl2+2C5H6=Fe(C5H5)2+2KCl+2H2O,其装置如下图所示。

实验步骤为:
①在三颈烧瓶中加入25 g粉末状的KOH,并从仪器a中加入60 mL无水乙醚,充分搅拌,同时通氮气约10 min;
②再从仪器a滴入5.5 mL新蒸馏的环戊二烯(C5H6,密度为0.95 g·cm-3),搅拌;
③将6.5 g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25 mL装入仪器a中,慢慢滴入三颈烧瓶中,45 min滴完,继续搅拌45 min;
④再从仪器a加入25 mL无水乙醚搅拌;
⑤将三颈烧瓶中的液体转入仪器X中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器a、X的名称分别是_____________。
(2)步骤①中通入氮气的原因是_____________(用化学方程式表示)。
(3)三颈烧瓶的适宜容积应为_________(选编号)。
①100 mL ②250 mL ③500 mL
(4)步骤⑤用盐酸洗涤的目的是_______________。
(5)步骤⑦是二茂铁粗产品的提纯,操作装置如图二所示,其操作名称为___________;该操作中棉花的作用是___________________。
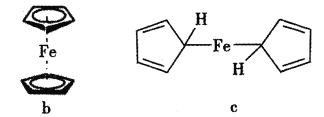
(6)为了确认得到的是二茂铁,还需要进行的一项简单实验是__________。确定二茂铁的结构是下图b而不是c,其测定的谱图为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,调节反应物用量或浓度不会改变反应产物的是( )
A.Fe与Cl2反应
B.CO2通入石灰水
C.HNO3中加入Cu
D.AlCl3溶液中滴入NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com