
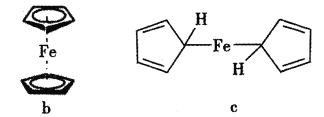
【题目】二茂铁是一种特殊的金属有机化合物,可用作燃料的节能消烟剂、抗爆剂等,熔点为173 ℃,在100 ℃时开始升华;沸点是249 ℃。实验室制备二茂铁的反应原理是:2KOH+FeCl2+2C5H6=Fe(C5H5)2+2KCl+2H2O,其装置如下图所示。

实验步骤为:
①在三颈烧瓶中加入25 g粉末状的KOH,并从仪器a中加入60 mL无水乙醚,充分搅拌,同时通氮气约10 min;
②再从仪器a滴入5.5 mL新蒸馏的环戊二烯(C5H6,密度为0.95 g·cm-3),搅拌;
③将6.5 g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25 mL装入仪器a中,慢慢滴入三颈烧瓶中,45 min滴完,继续搅拌45 min;
④再从仪器a加入25 mL无水乙醚搅拌;
⑤将三颈烧瓶中的液体转入仪器X中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器a、X的名称分别是_____________。
(2)步骤①中通入氮气的原因是_____________(用化学方程式表示)。
(3)三颈烧瓶的适宜容积应为_________(选编号)。
①100 mL ②250 mL ③500 mL
(4)步骤⑤用盐酸洗涤的目的是_______________。
(5)步骤⑦是二茂铁粗产品的提纯,操作装置如图二所示,其操作名称为___________;该操作中棉花的作用是___________________。
(6)为了确认得到的是二茂铁,还需要进行的一项简单实验是__________。确定二茂铁的结构是下图b而不是c,其测定的谱图为_____________。
【答案】恒压漏斗、分液漏斗 4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓ ② 除去多余的KOH 升华 防止二茂铁挥发进入空气中 测定所得固体的熔点 核磁共振氢谱
【解析】
(1)根据仪器的结构,结合仪器的用途确定仪器名称;
(2)二茂铁中铁是+2价,易被空气中氧气氧化,通入氮气排尽装置中空气;
(3)仪器c为三颈烧瓶,其中盛放液体的体积不超过容积的![]() 分析判断;
分析判断;
(4)盐酸可中和KOH生成KCl和水;
(5)二茂铁有固体直接变成气体,然后冷凝收集,称为升华;棉花团有防止粉末逸出的功能;
(6)可以通过测定所得固体的熔点确定;根据核磁共振氢谱图确定物质结构。
(1)根据装置图可知仪器a是恒压漏斗;仪器X用于分离互不相溶的两层液体物质,使用的是分液漏斗;
(2)二茂铁中铁是+2价,易被空气中氧气氧化,通入氮气排尽装置中空气,防止实验过程中亚铁离子被氧化;
(3)由题意可知三颈烧瓶中共加入液体112.5 mL,三颈烧瓶中盛放液体的体积不超过容积的![]() ,所以应该选择的规格是250 mL三颈烧瓶,故合理选项是②;
,所以应该选择的规格是250 mL三颈烧瓶,故合理选项是②;
(4)步骤⑤用盐酸洗涤,可与其中的KOH发生中和反应,而除去多余的KOH;
(5)二茂铁由固体直接变成气体,然后冷凝收集,其操作名称为升华;该操作中棉花的作用是防止二茂铁挥发进入空气中;
(6)为了确认得到的是二茂铁,还需要进行的一项简单实验是测定所得固体的熔点;可根据物质的核磁共振氢谱图确定物质结构是b还是c,若是b结构,分子中只有一种位置的H原子,只有1个吸收峰;若是图c结构,分子中含有3种不同位置的H原子,有3个吸收峰,吸收峰的面积比为1:2:2。


科目:高中化学 来源: 题型:
【题目】已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,不正确的是( )
A.原子序数:Y>X>Z>WB.离子半径:X+>Y2+>Z->W2-
C.原子最外层电子数:Z>W>Y>XD.还原性:X>Y,W2->Z-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在20.00 mL 0.10 mol/LCH3COOH溶液中滴入0.10 mol/LNaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
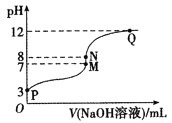
A.T℃时,CH3COOH的电离平衡常数Ka=1.0×10-3
B.M点对应的NaOH溶液的体积为20.00 mL
C.N点所示溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.N点与Q点所示溶液中水的电离程度:N>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AA705合金(含Al、Zn、Mg和Cu)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。但这种合金很难被焊接。最近科学家将碳化钛纳米颗粒(大小仅为十亿分之一米)注入AA7075的焊丝内,让这些纳米颗粒充当连接件之间的填充材料。注入了纳米粒子的填充焊丝也可以更容易地连接其他难以焊接的金属和金属合金。回答下列问题:
(1)基态铜原子的价层电子排布式为__________。
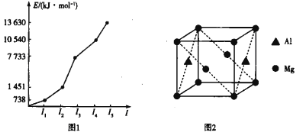
(2)第三周期某元素的前5个电子的电离能如图1所示。该元素是_____(填元素符号),判断依据是_______。
(3)CN—、NH3、H2O和OH—等配体都能与Zn2+形成配离子。1mol [Zn(NH3)4]2+含___ molσ键,中心离子的配位数为_____。
(4)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。1个铝原子周围有_____个镁原子最近且等距离。
(5)在二氧化钛和光照条件下,苯甲醇可被氧化成苯甲醛:
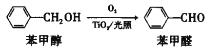
①苯甲醇中C原子杂化类型是__________。
②苯甲醇的沸点高于苯甲醛,其原因是__________。
(6)钛晶体有两种品胞,如图所示。
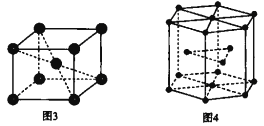
①如图3所示,晶胞的空间利用率为______(用含п的式子表示)。
②已知图4中六棱柱边长为x cm,高为y cm。该钛晶胞密度为D g·cm-3,NA为______mol—1(用含x y和D的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用闪锌矿(主要成分为ZnS,还含有CdS、Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:(已知Cd的金属活动性介于Zn和Fe之间)
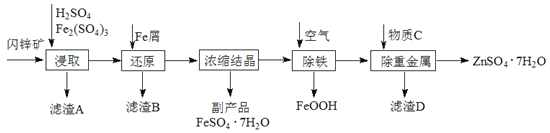
(1)从滤渣A中可获得一种淡黄色非金属单质的副产品,其化学式为________。
(2)浸取过程中Fe2(SO4)3的作用是_______________,浸取时Fe2(SO4)3与ZnS发生反应的化学方程式为____________________________________________。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为_______________________。该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是____________________________________。
(4)置换法除重金属离子是Cd2+,所用物质C为_________。
(5)硫酸锌的溶解度与温度之间的关系如下表:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
从除重金属后的硫酸锌溶液中获得硫酸锌晶体的实验操作为__________、__________、过滤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的叙述一定不正确的是
A. 向FeCl2溶液中滴加NH4SCN溶液,溶液显红色
B. KAl(SO4) 2·12H2O溶于水可形成 Al(OH)3胶体
C. NH4Cl与Ca(OH)2混合加热可生成NH3
D. Cu与FeCl3溶液反应可生成CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为一些物质之间的转化关系,其中部分反应中反应物或生成物未列全。已知A、H、I、K均为家庭厨房中的常见物质,其中A是食品调味剂,H是消毒剂的有效成分,I、K可用作食品发泡剂。B是一种有机酸盐,E、F、G均为氧化物,L是红褐色沉淀。

根据以上信息,回答下列问题:
(1)B的组成元素为_____。
(2)鉴别等物质的量浓度的I、K稀溶液的实验方法为_____。
(3)G→J的离子方程式为_____。
(4)M是含氧酸盐,反应①中H、L、D的物质的量之比为3:2:4,则M的化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以熔融的碳酸盐(K2CO3)为电解液,泡沫镍为电极,氧化纤维布为隔膜(仅允许阴离子通过)可构成直接碳燃料电池,其结构如图所示,下列说法正确的是
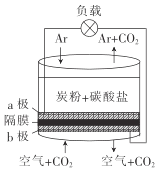
A.该电池工作时,CO32-通过隔膜移动到b极
B.若a极消耗1mol碳粉,转移电子数为4NA
C.b极的电极反应式为2CO2+O2-4e-=2CO32-
D.为使电池持续工作,理论上需要补充K2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com