
【题目】T℃时,在20.00 mL 0.10 mol/LCH3COOH溶液中滴入0.10 mol/LNaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
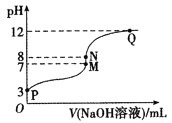
A.T℃时,CH3COOH的电离平衡常数Ka=1.0×10-3
B.M点对应的NaOH溶液的体积为20.00 mL
C.N点所示溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.N点与Q点所示溶液中水的电离程度:N>Q
【答案】D
【解析】
A. T℃时,0.10 mol/L CH3COOH溶液的pH=3,说明溶液中c(H+)=10-3 mol/L,则该温度下CH3COOH的电离平衡常数Ka=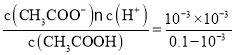 ≈10-5,A错误;
≈10-5,A错误;
B. M点溶液pH=7,若对应的NaOH溶液的体积为20.00 mL,则醋酸与NaOH恰好中和,溶液为CH3COONa,该盐是强碱弱酸盐,水解使溶液显碱性,与题干的溶液显中性相违背,说明M点对应的NaOH溶液的体积小于20.00 mL,B错误;
C. N点时所示溶液中醋酸与NaOH恰好中和,溶液为CH3COONa溶液,CH3COO-发生水解反应而消耗,所以c(Na+)>c(CH3COO-),CH3COO-发生水解反应消耗水电离产生的H+,最终达到平衡时,溶液中c(OH-)> c(H+),但盐水解程度是微弱的,水解产生的离子浓度远小于盐电离产生的离子浓度,因此c(CH3COO-)>c(OH-),故该溶液中离子浓度关系为:c(Na+)> c(CH3COO-)>c(OH-)>c(H+),C错误;
D. N点时所示溶液中醋酸与NaOH恰好中和,溶液中的溶质为CH3COONa,溶液中只有盐的水解作用,促进水的电离;而Q点时NaOH过量,溶液为CH3COONa和NaOH的混合液,由于NaOH电离产生OH-对水的电离平衡起抑制作用,使盐水解程度减小,故最终达到平衡时水的电离程度N>Q,D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】下列有关Na2CO3 和NaHCO3的说法错误的是
A. 等质量Na2CO3 和NaHCO3分别和足量盐酸反应,相同条件下前者生成CO2少
B. 将石灰水分别加入NaHCO3和Na2CO3中,前者不生成沉淀
C. 相同条件下Na2CO3 比NaHCO3更易溶于水
D. Na2CO3 固体中含少量NaHCO3,可用加热法除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用18.4molL-1的浓硫酸来配制480mL0.2molL-1的稀硫酸。可供选用的仪器有:①胶头滴管②烧瓶③烧杯④药匙⑤量筒⑥托盘天平⑦玻璃棒
请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有___(选填序号),还缺少的仪器有(写仪器名称)___。
(2)需要用量筒量取上述浓硫酸的体积为___mL,量取浓硫酸时应选用___(选填①10mL②50mL③100mL)规格的量筒。
(3)实验中两次用到玻璃棒,其作用分别是:___、___。
(4)下列对容量瓶及其使用方法的描述中正确的是___。
A.容量瓶上标有容积、温度和浓度
B.容量瓶用蒸馏水洗净后,必须烘干
C.配制溶液时,把量好的浓硫酸小心倒入容量瓶中,加入蒸馏水到接近刻度线1~2cm处,改用胶头滴管加蒸馏水至刻度线
D.使用前要检查容量瓶是否漏水
(5)在配制过程中,下列操作可引起所配溶液浓度偏低的有___(填序号)
①未洗涤稀释浓硫酸时用过的烧杯和玻璃棒
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知磷酸分子(![]() )中的三个氢原子都可与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。则下列说法正确的是
)中的三个氢原子都可与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。则下列说法正确的是
A.H3PO2在水溶液中发生电离:H3PO2![]() H++H2PO2-、H2PO2-
H++H2PO2-、H2PO2-![]() H++HPO22-
H++HPO22-
B.H3PO4属于三元酸、H3PO2属于二元酸
C.NaH2PO2属于酸式盐,其水溶液呈酸性
D.H3PO2具有较强的还原性,其结构式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告中提出“打赢蓝天保卫战”,对污染防治要求更高。某种利用垃圾渗透液实现发电、环保二位一体结合的装置示意图如下。当该装置工作时,下列说法正确的是
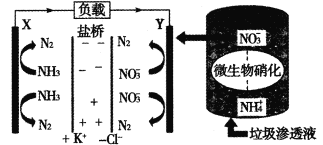
A.盐桥中Cl-向Y极移动
B.电路中流过7.5 mol电子时,共产生N2的体积为44.8 L(标况)
C.电流由X极沿导线流向Y极
D.Y极发生的反应为2NO3-+10e-+6H2O=N2↑+12OH-,周围pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃、101 kPa时某些物质的燃烧热数据如下:
名称 | 化学式 | ΔH (kJ/mol) | 名称 | 化学式 | ΔH (kJ/mol) |
石墨 | C(s) | 393.5 | 乙烷 | C2H6(g) | 1560 |
金刚石 | C(s) | 395.0 | 乙烯 | C2H4(g) | 1411 |
氢气 | H2(g) | 285.8 | 乙炔 | C2H2(g) | 1300 |
一氧化碳 | CO(g) | 283.0 | 乙醇 | C2H5OH(l) | 1367 |
(1)相同质量的上述八种物质,完全燃烧放热最多的名称是____。
(2)石墨与金刚石互为____。
a.同位素 b.同素异形体 c.同分异构体 d.同系物
常温常压下,二者更稳定的是___。(填中文名称)
(3)在标准状况下,22.4LCO和C2H2的混合气体在过量的氧气中完全燃烧放出1096.6 kJ的热,则燃烧产生的CO2的物质的量为___mol。
(4)估算在Ni作催化剂时,乙烯与氢气发生加成反应的焓变。C2H4(g)+H2(g)=C2H6(g) ΔH=____。
(5)已知破坏下列化学键需要吸收的能量如下:
C-C | C=C | H-H |
347kJ/mol | 619kJ/mol | 436kJ/mol |
根据(4)的结论,估算C-H键的键能为____kJ/mol。
a.322.5 b.422.5 c.522.5 d.622.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁是一种特殊的金属有机化合物,可用作燃料的节能消烟剂、抗爆剂等,熔点为173 ℃,在100 ℃时开始升华;沸点是249 ℃。实验室制备二茂铁的反应原理是:2KOH+FeCl2+2C5H6=Fe(C5H5)2+2KCl+2H2O,其装置如下图所示。

实验步骤为:
①在三颈烧瓶中加入25 g粉末状的KOH,并从仪器a中加入60 mL无水乙醚,充分搅拌,同时通氮气约10 min;
②再从仪器a滴入5.5 mL新蒸馏的环戊二烯(C5H6,密度为0.95 g·cm-3),搅拌;
③将6.5 g无水FeCl2与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25 mL装入仪器a中,慢慢滴入三颈烧瓶中,45 min滴完,继续搅拌45 min;
④再从仪器a加入25 mL无水乙醚搅拌;
⑤将三颈烧瓶中的液体转入仪器X中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器a、X的名称分别是_____________。
(2)步骤①中通入氮气的原因是_____________(用化学方程式表示)。
(3)三颈烧瓶的适宜容积应为_________(选编号)。
①100 mL ②250 mL ③500 mL
(4)步骤⑤用盐酸洗涤的目的是_______________。
(5)步骤⑦是二茂铁粗产品的提纯,操作装置如图二所示,其操作名称为___________;该操作中棉花的作用是___________________。
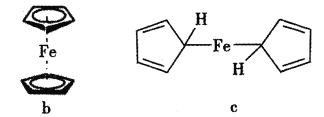
(6)为了确认得到的是二茂铁,还需要进行的一项简单实验是__________。确定二茂铁的结构是下图b而不是c,其测定的谱图为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组试利用镁铝合金废料(不含其它杂质)制备硫酸铝晶体,其实验流程如图:
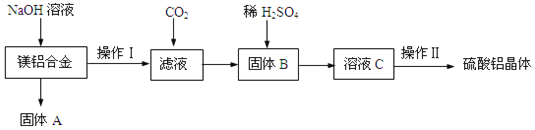
(1)在镁铝合金中加入NaOH溶液,发生反应的离子反应方程式为_____,固体B的化学式_____。
(2)操作Ⅱ包含的实验步骤有:_____、冷却结晶、过滤、洗涤、干燥。
(3)若初始时称取的镁铝合金废料的质量为7.65 g,得到固体A的质量为3.6 g,硫酸铝晶体的质量为49.95 g(假设每一步的转化率均为100%)。计算所得硫酸铝晶体的化学式为_____。( 在答题卷上写出计算过程)
(4)另取7.65 g该镁铝合金废料溶于400mL 3mol/L盐酸后,滴入3mol/LNaOH溶液,使所得沉淀中的Al(OH)3完全溶解,则滴入NaOH溶液的体积最少为_____mL(在答题卷上写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】格氏试剂(RMgX,X=Cl、Br、I)是一种重要的有机合成中间体,酯类化合物与格氏试剂的反应是合成叔醇类化合物的重要方法,由只含一种官能团的物质A制备E的合成路线如图,回答下列问题:

已知信息如下:
①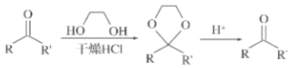
②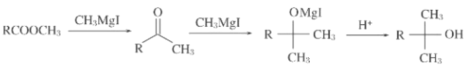
(1)A→B的反应类型为___,E的分子式为___。
(2)B中所含官能团的名称为___。
(3)C→D的化学方程式为___。
(4)M是比C多一个碳的C的同系物,同时满足下列条件的M的同分异构体有___种(不考虑立体异构)。
①含六元碳环结构,不含甲基;②能与NaHCO3溶液反应放出CO2;③能发生银镜反应。
写出其中核磁共振氢谱有七组峰,且峰面积的比是4∶4∶2∶1∶1∶1∶1的所有物质的结构简式___。
(5)将下列D→E的流程图补充完整:___。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com