
【题目】格氏试剂(RMgX,X=Cl、Br、I)是一种重要的有机合成中间体,酯类化合物与格氏试剂的反应是合成叔醇类化合物的重要方法,由只含一种官能团的物质A制备E的合成路线如图,回答下列问题:

已知信息如下:
①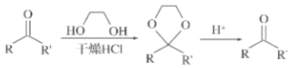
②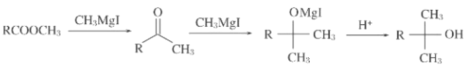
(1)A→B的反应类型为___,E的分子式为___。
(2)B中所含官能团的名称为___。
(3)C→D的化学方程式为___。
(4)M是比C多一个碳的C的同系物,同时满足下列条件的M的同分异构体有___种(不考虑立体异构)。
①含六元碳环结构,不含甲基;②能与NaHCO3溶液反应放出CO2;③能发生银镜反应。
写出其中核磁共振氢谱有七组峰,且峰面积的比是4∶4∶2∶1∶1∶1∶1的所有物质的结构简式___。
(5)将下列D→E的流程图补充完整:___。

【答案】氧化反应 C9H16O2 羰基、羧基  +H2O 9
+H2O 9  、
、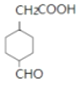 、
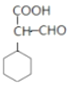
、
 、
、
【解析】
只含一种官能团的物质A(C7H14O2)能够被酸性高锰酸钾溶液氧化生成B(C7H10O3),B能够与甲醇发生酯化反应生成C,说明B中含有羧基;根据信息①,C与![]() 反应生成D,则C中含有羰基,根据信息②,结合E(
反应生成D,则C中含有羰基,根据信息②,结合E(![]() )的结构可知,D为
)的结构可知,D为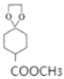 ,则C为
,则C为![]() ,B为
,B为![]() ,A为
,A为![]() ,据此分析解答。
,据此分析解答。
(1)酸性高锰酸钾溶液具有强氧化性,A(![]() )能够被酸性高锰酸钾溶液氧化生成B(
)能够被酸性高锰酸钾溶液氧化生成B(![]() );E(
);E(![]() )的分子式为C9H16O2,故答案为:氧化反应;C9H16O2;
)的分子式为C9H16O2,故答案为:氧化反应;C9H16O2;
(2)B为![]() ,所含官能团有羰基、羧基,故答案为:羰基、羧基;
,所含官能团有羰基、羧基,故答案为:羰基、羧基;
(3)根据信息①,C(![]() )与
)与![]() 反应生成D(
反应生成D( ),反应的化学方程式为
),反应的化学方程式为![]() +
+![]()
![]()
 +H2O,故答案为:
+H2O,故答案为:![]() +
+![]()
![]()
 +H2O;
+H2O;
(4)M是比C(![]() )多一个碳的C的同系物,则M的分子式为C9H14O3。①含六元碳环结构,不含甲基;②能与NaHCO3溶液反应放出CO2,说明M中含有羧基;③能发生银镜反应,说明M中还有醛基,满足上述条件的M中含有六元脂环结构、羧基和醛基,则①含有
)多一个碳的C的同系物,则M的分子式为C9H14O3。①含六元碳环结构,不含甲基;②能与NaHCO3溶液反应放出CO2,说明M中含有羧基;③能发生银镜反应,说明M中还有醛基,满足上述条件的M中含有六元脂环结构、羧基和醛基,则①含有![]() 、—CH2COOH、—CHO的有4种,②含有
、—CH2COOH、—CHO的有4种,②含有![]() 、—COOH、—CH2CHO的有4种;③
、—COOH、—CH2CHO的有4种;③ ,共9种;其中核磁共振氢谱有七组峰,且峰面积的比是4∶4∶2∶1∶1∶1∶1的有
,共9种;其中核磁共振氢谱有七组峰,且峰面积的比是4∶4∶2∶1∶1∶1∶1的有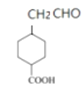 、
、 、
、 ,故答案为:9;
,故答案为:9; 、
、 、
、 ;
;
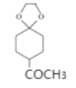
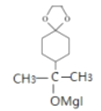
(5)根据信息②,D( )首先在CH3MgI作用下反应生成
)首先在CH3MgI作用下反应生成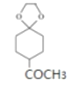 ,
, 再在CH3MgI作用下反应生成
再在CH3MgI作用下反应生成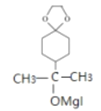 ,
, 酸化生成E(
酸化生成E(![]() ),故答案为:
),故答案为: 、
、 。
。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】T℃时,在20.00 mL 0.10 mol/LCH3COOH溶液中滴入0.10 mol/LNaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。下列说法正确的是
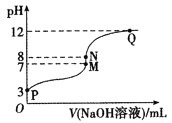
A.T℃时,CH3COOH的电离平衡常数Ka=1.0×10-3
B.M点对应的NaOH溶液的体积为20.00 mL
C.N点所示溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.N点与Q点所示溶液中水的电离程度:N>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为一些物质之间的转化关系,其中部分反应中反应物或生成物未列全。已知A、H、I、K均为家庭厨房中的常见物质,其中A是食品调味剂,H是消毒剂的有效成分,I、K可用作食品发泡剂。B是一种有机酸盐,E、F、G均为氧化物,L是红褐色沉淀。

根据以上信息,回答下列问题:
(1)B的组成元素为_____。
(2)鉴别等物质的量浓度的I、K稀溶液的实验方法为_____。
(3)G→J的离子方程式为_____。
(4)M是含氧酸盐,反应①中H、L、D的物质的量之比为3:2:4,则M的化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,下列反应的平衡常数数值如下:2NO(g) ![]() N2(g)+O2(g) K1=1×1030 2H2(g)+O2(g)
N2(g)+O2(g) K1=1×1030 2H2(g)+O2(g) ![]() 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
2CO2(g) ![]() 2CO(g)+O2(g) K3=4×10-92 以下说法正确的是
2CO(g)+O2(g) K3=4×10-92 以下说法正确的是
A.常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)·c(O2)/ c(NO)
B.常温下,NO、H2O、CO2三种化合物分解放出O2的进行程度由大到小的顺序为NO>H2O>CO2
C.常温下,水分解产生O2,此时平衡常数的数值约为5×10-80
D.以上说法都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能充分说明可逆反应N2(g)+O2(g)![]() 2NO(g)已达到平衡状态的是( )
2NO(g)已达到平衡状态的是( )
A. 容器内压强不随时间改变
B. 容器内反应物总物质的量不随时间改变
C. 容器内气体N2、O2、NO的分子数之比为1:1:2
D. 单位时间内每消耗n mo1N2,同时生成2n mo1NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.28g乙烯和丙烯中的极性键数目为4NA
B.1.0molCH4与Cl2在光照下反应生成CH3Cl分子数为1.0NA
C.1mol氖气中含有的原子总数为2NA
D.0.1L0.1molL-1MgCl2溶液中的Mg2+数目为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以熔融的碳酸盐(K2CO3)为电解液,泡沫镍为电极,氧化纤维布为隔膜(仅允许阴离子通过)可构成直接碳燃料电池,其结构如图所示,下列说法正确的是
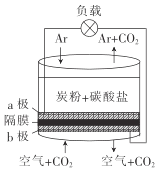
A.该电池工作时,CO32-通过隔膜移动到b极
B.若a极消耗1mol碳粉,转移电子数为4NA
C.b极的电极反应式为2CO2+O2-4e-=2CO32-
D.为使电池持续工作,理论上需要补充K2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向2L密闭容器中加入2molN2和10molH2,发生反应N2(g)+3H2(g)![]() 2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
2NH3(g),2min时测得剩余N2为1mol,下列化学反应速率表示不正确的是( )
A. v(N2)=0.25 mol·L-1·min-1
B. v(H2)=0.75 mol·L-1·min-1
C. v(NH3)=1 mol·L-1·min-1
D. v(NH3)=0.5 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O(g)=CO(g)ΔH1 ; C(s)+![]() O2(g)=CO(g) ΔH2
O2(g)=CO(g) ΔH2
②S(s)+O2 (g)=SO2 (g) ΔH3 ; S(g)+O2 (g)=SO2 (g) ΔH4
③H2(g)+ ![]() O2(g)=H2O(l) ΔH5;2H2(g)+O2(g)=2H2O(l) ΔH6
O2(g)=H2O(l) ΔH5;2H2(g)+O2(g)=2H2O(l) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7;CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8
A. ①B. ④C. ②③④D. ①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com