
【题目】下列叙述错误的是( )
A.用新制的银氨溶液可区分甲酸甲酯和乙醛
B.用高锰酸钾酸性溶液可区分己烷和3﹣己烯
C.用水可区分苯和溴苯
D.用金属钠可区分乙醇和乙醚
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】下列变化一定属于化学变化的是( ) ①导电②爆炸③缓慢氧化④SO2使品红溶液褪色⑤无水硫酸铜由白变蓝⑥工业制O2⑦白磷转化为红磷 ⑧久置浓硝酸变黄⑨16O与18O间的相互转化.
A.②③④⑦⑧⑨
B.③④⑤⑦⑧
C.②③⑥⑦⑨
D.④⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:

请回答下列问题:
(1)若A为H2O(g),可以得到Fe3O4,写出H2O的电子式:________________。
(2)若B为NaClO3与稀硫酸,写出其氧化Fe2+生成Fe3+的离子方程式___________________。
(3)若C为KNO3和KOH的混合物,写出其与Fe2O3加热共熔制得高铁酸钾的化学方程式,并配平:___________
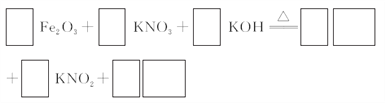
(4)为测定溶液Ⅰ中铁元素的总含量,实验操作如下:准确量取20.00 mL溶液Ⅰ于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用0.1 00 0 mol·L-1 Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00 mL。
已知:2Fe3++2I-===2Fe2++I2 ;I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() 。
。
①写出滴定选用的指示剂________,滴定终点观察到的现象_______________________。
②溶液Ⅰ中铁元素的总含量为__________g·L-1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )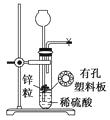
①食盐水②KNO3溶液③适量稀硫酸铜溶液
④Na2CO3溶液⑤CCl4⑥浓氨水
A.①③⑤
B.②⑥
C.③⑤
D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验。 
(1)比较两实验装置,图2所示装置的优点是: ①能更好地吸收有毒气体SO2 , 防止其污染环境;
②。
(2)能说明有SO2气体产生的实验现象是?
(3)反应一段时间后,用滴管吸取A试管中的溶液滴入适量水中为试样,试样中所含金属离子的成分有以下三种可能: Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+。
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空白:
A.稀盐酸溶液 B.稀硫酸溶液
C.KSCN溶液 D.KMnO4溶液
E.NaOH溶液 F.淀粉KI溶液
G.H2O2溶液
验证Ⅱ:取试样,先滴加少量的(填试剂序号,下同),振荡,再滴加少量的 , 根据溶液颜色的变化可确定假设Ⅱ是否正确。
验证Ⅲ:步骤1.取试样,滴加少量的(填试剂序号),溶液的颜色变色则试样中含有Fe3+ , 发生反应的离子方程式为。
步骤2.再取适量的试样滴加到少量的(填试剂序号),溶液的颜色变为色,则试样中含有Fe2+。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中含有流失的生产用料、中间产物和产品,以及生产过程中产生的污染物.随着工业的迅速发展,废水的排放量迅速增加,严重威胁人类的健康和安全,工业废水的处理比城市污水的处理更为重要.图是含铬工业废水和含氰废水的处理流程: 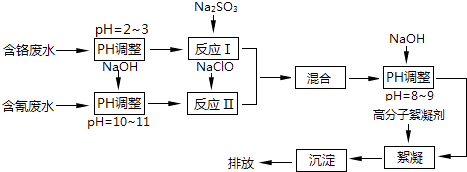
请回答下列问题:
(1)电镀废水中的铬主要以CrO42﹣形式存在,其中Cr元素的化合价为 .
(2)酸性条件下,CrO42﹣极易被还原剂还原为毒性较小的Cr3+ . 图中“反应Ⅰ”的离子方程式为 .
(3)pH>10时,“反应Ⅱ”中的NaClO可快速地将氰离子(CN﹣)氧化为无毒的两种物质,这两种物质是、(写化学式);若pH<8.5,则生成剧毒的CNCl气体(沸点13.1℃),写出该反应的离子方程式 .
(4)经过“反应Ⅰ”和“反应Ⅱ”将两种废水混合的目的是 .
(5)含氰废水及含铬废水可以通过电化学的方法进行无害化处理. ①可采用惰性电极对含氰废水进行电解,氰离子在碱性条件下被氧化为无毒的物质,该电解工艺中,阳极电极反应是 .
②电解法处理酸性含铬废水(若铬元素以Cr2O72﹣形式存在)时,以铁板和石墨作电极,处理过程中存在反应Cr2O72﹣+6Fe2++14H+=2Cr3++6Fe3++7H2O.则阳极的电极反应式为 , 当有1mol Cr2O72﹣被还原时,电路中转移的电子为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在家自制“84消毒液”,他根据84消毒液标签上的配方,用NaC1O固体配制480mL质量分数为25%的、密度为1.19g/cm3的NaC1O消毒液.下列说法正确的是( )
A.容量瓶用蒸馏水洗净后需晾干才能使用
B.需称取NaClO固体144g
C.所配得NaClO消毒液久置后会失效
D.8 4消毒液的消毒原理是利用了NaClO的强碱性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com