
【题目】铁及其化合物有重要用途,如聚合硫酸铁[Fe2(OH)n(SO4)3-n/2]m是一种新型高效的水处理混凝剂,而高铁酸钾(其中铁的化合价为+6)是一种重要的杀菌消毒剂,某课题小组设计如下方案制备上述两种产品:

请回答下列问题:
(1)若A为H2O(g),可以得到Fe3O4,写出H2O的电子式:________________。
(2)若B为NaClO3与稀硫酸,写出其氧化Fe2+生成Fe3+的离子方程式___________________。
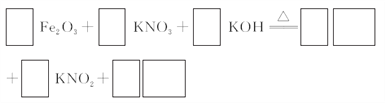
(3)若C为KNO3和KOH的混合物,写出其与Fe2O3加热共熔制得高铁酸钾的化学方程式,并配平:___________
(4)为测定溶液Ⅰ中铁元素的总含量,实验操作如下:准确量取20.00 mL溶液Ⅰ于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用0.1 00 0 mol·L-1 Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00 mL。
已知:2Fe3++2I-===2Fe2++I2 ;I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() 。
。
①写出滴定选用的指示剂________,滴定终点观察到的现象_______________________。
②溶液Ⅰ中铁元素的总含量为__________g·L-1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会________(填“偏高”“偏低”或“不变”)。
【答案】 略 6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O 略 淀粉 滴加最后一滴标准液溶液蓝色消失且半分钟不恢复 5.6 偏高
【解析】(1) H2O的电子式为:![]() ;(2) NaClO3在酸性条件下将Fe2+氧化生成Fe3+的离子方程式为:6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O;(3)KNO3和KOH的混合物,写出其与Fe2O3加热共融制得K2FeO4,则缺项中有一种为K2FeO4,K2FeO4中铁元素化合价为+6,则铁离子从+3价变为+6价,化合价升高3价,化合价至少升高3×2=6价;KNO3中N元素从+5降为KNO2中的+3价,化合价降低2价,则化合价最小公倍数为6,所以氧化铁的系数为1,KNO3的系数为3,然后根据质量守恒定律配平,配平后的方程式为:Fe2O3+3KNO3+2KOH=K2FeO4+3KNO2+H2O;(4) ①Fe3+氧化I-生成I2,淀粉遇碘变蓝,选择淀粉溶液作指示剂;滴加最后一滴标准液溶液蓝色消失且半分钟不恢复说明是终点,②若滴定前溶液中H2O2没有除尽,过量的H2O2氧化KI得到I2,根据关系式2Fe3+~I2,I2的量增大使所测定的铁元素的含量偏高。
;(2) NaClO3在酸性条件下将Fe2+氧化生成Fe3+的离子方程式为:6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O;(3)KNO3和KOH的混合物,写出其与Fe2O3加热共融制得K2FeO4,则缺项中有一种为K2FeO4,K2FeO4中铁元素化合价为+6,则铁离子从+3价变为+6价,化合价升高3价,化合价至少升高3×2=6价;KNO3中N元素从+5降为KNO2中的+3价,化合价降低2价,则化合价最小公倍数为6,所以氧化铁的系数为1,KNO3的系数为3,然后根据质量守恒定律配平,配平后的方程式为:Fe2O3+3KNO3+2KOH=K2FeO4+3KNO2+H2O;(4) ①Fe3+氧化I-生成I2,淀粉遇碘变蓝,选择淀粉溶液作指示剂;滴加最后一滴标准液溶液蓝色消失且半分钟不恢复说明是终点,②若滴定前溶液中H2O2没有除尽,过量的H2O2氧化KI得到I2,根据关系式2Fe3+~I2,I2的量增大使所测定的铁元素的含量偏高。


科目:高中化学 来源: 题型:
【题目】(1)为了检验和除去下表中的各种杂质(括号里的为杂质),请从①中选出适当的检验试剂,从②中选出适当的除杂试剂,将所选的答案用字母填入相应的空格内。
物质 | 检验试剂 | 除杂试剂 |
(Ⅰ)甲烷(乙烯) | ________。 | ________。 |
(Ⅱ)酒精(水) | ________。 | ________。 |
①检验试剂:
A.无水硫酸铜 B.酸性高锰酸钾溶液
C.水 D.氢氧化钠溶液
②除杂试剂:
a.无水硫酸铜 b.乙酸
c.新制的生石灰 d.溴水
除杂时,乙烯发生反应的化学方程式为____________________。
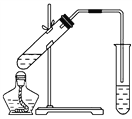
(2)如图,在左试管中先加入2 mL 95%的乙醇,并在摇动下缓缓加入3 mL浓硫酸,再加入2 mL乙酸,充分摇匀。按图连接好装置,用酒精灯对左试管小火加热3~5 min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
试回答:
在右试管中通常加入________溶液,实验生成的乙酸乙酯,其密度比水________,是有特殊香味的液体。分离右试管中所得乙酸乙酯的操作为(只填名称)________。反应中加入浓硫酸的作用是_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组对生石灰与水反应是显著放热反应进行了实验探究,在除了用手触摸试管壁感觉发热外,还设计了下列几个可行性方案。
甲方案:将温度计与盛放有生石灰的小试管用橡皮筋捆绑在一起,放入有水的小烧杯中,用胶头滴管向小试管中缓缓滴入水,观察到的现象是_________、____________、________。说明反应放热。

乙方案:将盛放有生石灰的小试管插入带有支管的试管中,支管接①,用胶头滴管向小试管中缓缓滴入水,①中看到的现象是________________________________________,说明该反应放热。
丙方案:盛放有生石灰且带支管的试管中,支管接的导管中盛适量无水硫酸铜粉末,看到的现象是___________________________,说明反应放热,原因是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:
(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质.处理C物质可得到有价值的化学品,写出其中1种酸和1种盐的名称 .
(2)若B是气态氢化物.C、D是氧化物且会造成光化学烟雾污染.B与C在一定条件下反应生成的A是大气主要成分,写出该反应的化学方程式 .
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体.判断单质A的元素在周期表中的位置是 .写④反应离子方程式 .
(4)若A是太阳能电池用的光伏材料.C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性.写出②反应的化学方程式 .D的化学式是 .
(5)若A是应用最广泛的金属.④反应用到A,②⑤反应均用到同一种非金属单质.C的溶液用于蚀刻印刷铜电路板,写该反应的离子方程式 .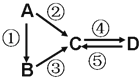
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块钠投入到盛有100mL硫酸铜溶液的烧杯里,不可能观察到的现象是( )
A.钠熔成小球并在液面上四处游动B.有气体产生
C.烧杯底部有红色的物质生成D.溶液有蓝色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 摩尔是物质的量的单位
B. 电子转移是氧化还原反应的本质
C. 熔融状态下或水溶液中能导电的化合物称为电解质
D. 得电子的物质被还原,是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.用新制的银氨溶液可区分甲酸甲酯和乙醛
B.用高锰酸钾酸性溶液可区分己烷和3﹣己烯
C.用水可区分苯和溴苯
D.用金属钠可区分乙醇和乙醚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解。请你和他一起通过图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。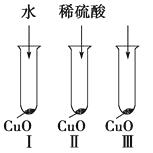
(1)该同学提出的假设是。
(2)通过实验Ⅰ可以证明。
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步所做的确认实验为:在Ⅲ中先加入溶液,再加入溶液。
(4)探究结果为。你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图,实验桌上放置的两容器中有等体积的甲、乙两种液体。几天后,两者的体积都明显减少,且甲比乙减少得多。由此现象得出的正确结论是( )
甲 乙
A.甲比乙易挥发
B.甲的沸点比乙高
C.甲的熔点比乙小
D.甲与乙都能挥发
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com