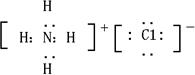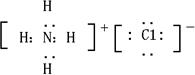(2008?开封一模)t℃时,将2mol N
2和1mol H
2通入体积为2L的恒温容密闭容器中,发生如下反应:N
2(g)+3H
2(g)?2NH
3(g);△H<0.2min后反应达到平衡,此时测得NH
3的物质的量为0.2mol.请填写下列空白:
(1)从反应开始至达到化学平衡,生成NH
3的平均反应速率为
0.05mol/(L?min)
0.05mol/(L?min)
;平衡时N
2转化率为
5%
5%
.
(2)下列叙述能证明该反应已经达到化学平衡状态的是(填标号,下同)
ABE
ABE
.
A.容器内压强不再发生变化
B.H
2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗n mol N
2的同时消耗3n mol H
2E.相同时间内消耗n mol N
2的同时消耗2n mol NH
3F.容器内气体的密度不再发生变化
(3)反应达平衡后,以下操作将引起平衡向正反应方向移动,并能提高N
2转化率的是:
BD
BD
A.向容器中通入少量N
2B.向容器中通入少量H
2C.使用催化剂
D.降低温度
E.向容器中通入少量氦气(已知氦气和N
2、H
2、NH
3都不发生反应)
(4)维持上述恒温恒容条件步变,若起始加入a mol N
2、b mol H
2、c mol NH
3,反应向逆方向进行,平衡时NH
3的物质的量仍然为0.2mol,则c的取值范围是
.
(5)保持温度不变,使体积缩小为原来的一半,则N
2的体积分数
增大
增大
(填“增大”“减小”或“不变”).请通过计算证明你的结论.
N
2(g)+3H
2(g)?2NH
3(g)
原平衡 1.9 0.7 0.2
转化x3x2x
新平衡 1.9-x 0.7-3x 0.2+2x
W(N
2后)-W(N
2前)=
-
=
,因x≤0.35,所以
>O
N
2(g)+3H
2(g)?2NH
3(g)
原平衡 1.9 0.7 0.2
转化x3x2x
新平衡 1.9-x 0.7-3x 0.2+2x
W(N
2后)-W(N
2前)=
-
=
,因x≤0.35,所以
>O
.



 阅读快车系列答案
阅读快车系列答案 (2008?开封一模)短周期元素的常见单质A、B、C、D在通常状况下均为气态,其中B分子中共价键最多,单质A分别与B、C、D在一定条件下发生反应,得到相应的共价化合物E、F、G,通常状况下F为液体,E、G为气体,且E与G可反应得到离子化合物H,H中的阳离子含有10个电子,阴离子含有18个电子.
(2008?开封一模)短周期元素的常见单质A、B、C、D在通常状况下均为气态,其中B分子中共价键最多,单质A分别与B、C、D在一定条件下发生反应,得到相应的共价化合物E、F、G,通常状况下F为液体,E、G为气体,且E与G可反应得到离子化合物H,H中的阳离子含有10个电子,阴离子含有18个电子.