
(1)已知在 2 L 的容器中进行下列可逆反应,各物质的有关数据如下:
aA (g)+ bB (g) ![]() 2C(g)
2C(g)
起始物质的量(mol): 3 2 0
2s末物质的量浓度(mol/L): 0.9 0.8 0.4
则① a = ,b = ;
② 2S内B的反应速率= 。
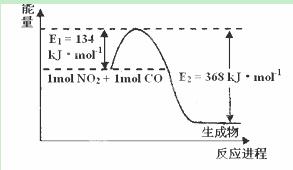
(2) 1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO
反应的热化学方程式 。
科目:高中化学 来源:志鸿系列必修一训练化学苏教版 苏教版 题型:022
(1)完成下列填空:
①已知在0.5 L NaCl溶液中含有0.5 mol NaCl,则1 LNaCl溶液中含NaCl________mol.
②已知在2 L NaOH溶液中含有4 mol NaOH,则1 L NaCl溶液中含NaOH________mol.
③已知在4 L H2SO4溶液中含有12 mol H2SO4,则1 L H2SO4溶液中含H2SO4________mol.
(2)三种不同溶液的计算结果,都表达了溶液的体积和溶质的物质的量的什么关系?
查看答案和解析>>
科目:高中化学 来源:志鸿系列训练必修一化学人教版 人教版 题型:022
完成下列填空:
①已知在0.5 L NaCl溶液中含有0.5 mol NaCl,则1 L NaCl溶液中含NaCl________mol.
②已知在2 L NaOH溶液中含有4 mol NaOH,则1 L NaCl溶液中含NaOH________mol.
③已知在4 L H2SO4溶液中含有12 mol H2SO4,则1 L H2SO4溶液中含H2SO4________mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
①已知在
②已知在
③已知在
(2)三种不同溶液的计算结果,都表达了溶液的体积和溶质的物质的量的什么关系?
查看答案和解析>>
科目:高中化学 来源:2013-2014学年云南省毕业生复习统一检测理综化学试卷(解析版) 题型:填空题
2013年12月2日,我国在西昌卫星发射中心用“长征三号甲”运载火箭将“嫦娥三号”探月卫星成功送入太空,进一步向广寒宫探索。“长征三号甲”是三级液体助推火箭,一、二级为常规燃料,常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。
Ⅰ.常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。但有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) △H = -543kJ·mol-1
 H2(g)+
H2(g)+  F2(g)
= HF(g) △H = -269kJ·mol-1
F2(g)
= HF(g) △H = -269kJ·mol-1
H2(g)+  O2(g)
= H2O(g) △H = -242kJ·mol-1
O2(g)
= H2O(g) △H = -242kJ·mol-1
请写出肼和氟气反应的热化学方程式:_____________________________。
Ⅱ.氧化剂二氧化氮可由NO和 O2生成,已知在2 L密闭容器内,800 ℃时反应:
2NO(g)+O2(g) 2NO2(g)
ΔH 的体系中,n(NO)随时间的变化如表:
2NO2(g)
ΔH 的体系中,n(NO)随时间的变化如表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)(mol) |
0.200 |
0.100 |
0.080 |
0.050 |
0.050 |
0.050 |
|
n(O2)(mol) |
0.100 |
0.050 |
0.040 |
0.025 |
0.025 |
0.025 |
(1) 已知:K800℃>K1000℃,则该反应的ΔH ______0(填“大于”或“小于”),用O2表示从0~2 s内该反应的平均速率为__________。
(2)能说明该反应已达到平衡状态的是________。
a.容器内颜色保持不变 b. 2v逆(NO)=v正(O2)
c.容器内压强保持不变 d.容器内密度保持不变
(3)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有 。
(4)在上述条件下,计算通入2 mol NO和1 mol O2的平衡常数K=______________。
(5)在上述条件下,若开始通入的是0.2 mol NO2气体,达到化学平衡时,则NO2的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com