
若NA为阿伏伽德罗常数的值。下列叙述正确的是
A.1.0L1.0mol/L的NaAlO2水溶液中含有的氧原子数为2 NA
B.1mol Na被完全氧化,生成Na2O和Na2O2的混合物时,失去 NA个电子
C.1L 0.1mol/L的FeCl3溶液完全水解后所得胶粒的数目为0.1 NA
D.1mol的羟基与1 mol的氢氧根离子所含电子数均为9NA
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源:2015-2016学年江西省高一上第一次月考化学试卷(解析版) 题型:选择题
由CH4和O2组成的混合气体,标准状况下的密度为1 g·L-1,则该混合气体中CH4和O2的质量比为
A.3:4 B.1:2 C.2:3 D.3:2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高一上学期10月月考化学试卷(解析版) 题型:选择题
苯作萃取剂,并用分液漏斗萃取溴水中的溴单质的实验,下列说法正确的是
A.不能使用酒精作为萃取剂,因为溴单质在酒精中的溶解度比在水中的小
B.静置分层后有色层在下层,水层几乎无色
C.分液漏斗使用前应当用蒸馏水检验是否漏液
D.振荡、静置分层后,依次用两个不同的烧杯从下口分别接取上下两层液体
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江双鸭山第一中学高三上学期期中测试化学试卷(解析版) 题型:填空题
(14分)元素周期表的用途广泛。
(1)用“>”或“<”填空:
离子半径 | 非金属性 | 酸性 | 沸点 |
K+_____S2- | N____O | 硫酸_____高氯酸 | HF____HCl |
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是 (填序号)。
a.Cl2、Br2、I2的熔点 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d. HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液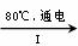 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
①完成I中反应的总化学方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中转化的基本反应类型是 ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是 。
(4)一定条件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如右图所示。
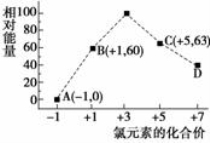
①D是 (填离子符号)。
②B→A+C反应的热化学方程式为 (用离子符号表示)
查看答案和解析>>
科目:高中化学 来源:2016届广东省揭阳市高三上学期第二次月考化学试卷(解析版) 题型:选择题
如图进行实验,试管中现象对应的离子方程式不正确的是
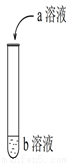
选项 | a | b | 试管中现象 | 离子方程式 |
A | 硫酸 | KI淀粉 | 在空气中放置一段时间后溶液呈蓝色 | 4H++ 4I- + O2=2I2 + 2H2O |
B | 稀盐酸 | Na2CO3 | 开始时无气泡,后来有气泡 | CO HCO |
C | 稀盐酸 | Na2SiO3 | 产生白色胶状物 | 2H++ SiO |
D | 硫酸 | 滴有酚酞Ba(OH)2 | 有白色沉淀生成,溶液由红色变为无色 | Ba2+ + OH- + H+ + SO BaSO4↓ + H2O |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北京大学附属中学分校高一上抽考化学试卷(解析版) 题型:选择题
在无色溶液中,能大量共存的离子组是
A.Cu2+、Cl-、Ba2+、Na+
B.K+. HCO3-、OH-、Cl-
C.Mg2+、Na+、Cl-、SO42-
D.K+、Mg2+、OH-、NO3-
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期期中测试化学试卷(解析版) 题型:选择题
一定条件下,中学化学常见物质甲、乙之间存在如下转化关系,Z是
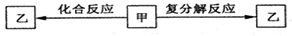
A.HCl B.FeCl2 C.KOH D.NaHCO3
查看答案和解析>>
科目:高中化学 来源:2016届广东省高三上学期第二次教学质检化学试卷(解析版) 题型:填空题
[化学——选修2:化学与技术](14分)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系, 在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
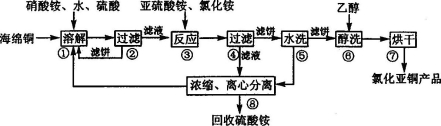
回答下列问题:
(1)步骤①中得到的氧化产物是 。溶解温度应控制在60~70℃,原因是 。
(2)写出步骤③中主要反应的离子方程式 。
(3)步骤⑤包括用pH = 2的酸洗、水洗两步操作,酸洗采用的酸是__________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是 。
(5)步骤②、④、⑤、⑧都要进行固液分离。工业上常用的固液分离设备有 (填字母)。
A.分馏塔 8.离心机 C.反应釜 D.框式压滤机
(6)准确称取所制备的氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O72-被还原为Cr3+。样品中CuCl的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南华侨中学高二上会考模拟化学试卷(解析版) 题型:选择题
不同国家垃圾的分类方法不同。我国国家标准《城市生活垃圾分类标准》中有六个粗分的一级类别和八个细分的二级类别。下列标志属于垃圾可回收标志的是

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com