
工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3气体,已知该反应为放热反应。现将2 mol SO2、1 mol O2充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO2的转化率为50%,则下列热化学方程式正确的是
A.2SO2(g)+O2(g)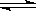 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
B.2SO2(g)+O2(g)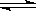 2SO3(g) ΔH=-98.3 kJ·mol-1
2SO3(g) ΔH=-98.3 kJ·mol-1
C.SO2(g)+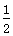 O2(g)
O2(g)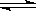 SO3(g) ΔH=+98.3 kJ·mol-1
SO3(g) ΔH=+98.3 kJ·mol-1
D.SO2(g)+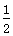 O2(g)
O2(g)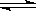 SO3(g) ΔH=-196.6 kJ·mol-1
SO3(g) ΔH=-196.6 kJ·mol-1
A
【解析】
试题分析:将2mol SO2、1mol O2充入一密闭容器中充分反应后,放出热量98.3kJ,此时测得SO2的物质的量为1mol,说明反应是可逆反应,不能进行彻底,实际发生反应的二氧化硫为1mol,1mol二氧化硫全部反应放热98.3KJ,热化学方程式为:2SO2(g)+O2(g)?2SO3(g)△H=-196.6 kJ?mol-1或SO2(g)+ O2(g)?SO3(g)△H=-98.3 kJ?mol-1;A、选项中的热化学方程式符合题意,故A正确;B、选项中的热化学方程式中反应热和对应二氧化硫的量不符合,故B错误;C、反应是放热反应,故C错误;D、反应是放热反应,故D错误;
O2(g)?SO3(g)△H=-98.3 kJ?mol-1;A、选项中的热化学方程式符合题意,故A正确;B、选项中的热化学方程式中反应热和对应二氧化硫的量不符合,故B错误;C、反应是放热反应,故C错误;D、反应是放热反应,故D错误;
考点:热化学方程式的书写


科目:高中化学 来源:2015届福建省高三上学期半期考试化学试卷(解析版) 题型:选择题
不能用于判断金属失电子能力强弱的是
A.同主族金属元素原子半径大小
B.1 mol金属单质在反应中失去电子的多少
C.水溶液中金属间发生的置换反应
D.金属元素最高价氧化物对应水化物的碱性强弱
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中化学试卷(解析版) 题型:选择题
分类方法在化学学科的发展中起到了非常重要的作用。下图是某反应在密闭容器中反应前后的分子状况示意图,“●”和“○”分别表示不同的原子。对此反应的分类一定不正确的是

A.化合反应
B.氧化还原反应
C.可逆反应
D.置换反应
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期半期联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期半期联考化学试卷(解析版) 题型:选择题
可用于电动汽车的铝?空气燃料电池,通常以NaCl溶液或NaOH溶液为电解质溶液,铝合金为负极,空气电极为正极。下列说法正确的是
A.以NaOH溶液为电解质溶液时,电池在工作过程中电解液的pH保持不变
B.以NaOH溶液为电解质溶液时,负极反应为:Al+3OH--3e-===Al(OH)3↓
C.以NaCl溶液或NaOH溶液为电解质溶液时,正极反应都为:O2+2H2O+4e-===4OH-
D.电池工作时,电子通过外电路从正极流向负极
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期半期联考化学试卷(解析版) 题型:实验题
(15分)某兴趣小组用下图装置探究氨的催化氧化。(三氧化二铬作催化剂)
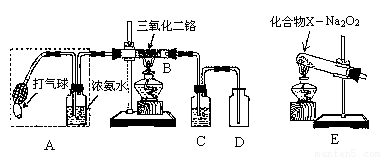
(1)氨催化氧化的化学方程式为 _________________________________________。
(2)加热玻璃管B一段时间后,挤压A中打气球鼓入空气,观察到B中物质呈红热状态;停止加热后仍能保持红热,该反应是_______反应(填“吸热”或“放热”)。
(3)为保证在装置D中观察到红棕色气体,装置C应装入_____________;若取消C,在D中仅观察到大量白烟,原因是_________________________。
(4)为实现氨催化氧化,也可用装置E替换装置_____________(填装置代号);化合物X为___________(填化学式只写一种),Na2O2的作用是__________________。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期半期联考化学试卷(解析版) 题型:选择题
某一无色溶液,若向其中加入足量饱和氯水,溶液呈橙黄色;再向橙黄色溶液中滴加BaCl2溶液,产生白色沉淀;若向原溶液中加入铝粉,有气体放出。该溶液可能大量存在的一组离子是
A.K+、H+、 、Na+ B.H+、Br-、
、Na+ B.H+、Br-、 、K+
、K+
C. 、Br-、OH-、Fe2+ D.H+、Br-、
、Br-、OH-、Fe2+ D.H+、Br-、 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源:2015届福建省高一上学期半期联考化学试卷(解析版) 题型:填空题
A、B、C是三种元素的原子,质子数都小于18。A原子与B原子的最外层电子数都是6,A原子与C原子的核外电子层数都为3, C原子的质子数比A少4。回答下列问题:
(1)A、B、C的元素符号分别为________、________、________;
(2)A的离子结构示意图为________;A与C组成的化合物为________(用具体元素符号表示);
(3)C单质与稀盐酸反应的化学方程式为__________________________;
(4)元素A的一种质量数为32的核素,与元素B的一种核素构成微粒为AB42-,1mol AB42-的质量为104g,则元素B的该核素中的中子数为 。
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:选择题
下列有关物质的性质和该性质的应用均正确的是( )
A.SiO2具有较好的导电性,可用于制造半导体材料
B.H2O2是一种绿色氧化剂,可氧化酸性高锰酸钾而产生O2
C.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸
D.Mg在空气中燃烧发出耀眼的白光,可用于制作信号弹
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com