
碳族元素包括:C、Si、 Ge、 Sn、Pb。
(1)碳纳米管有单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过杂化与周围碳原子成键,多层碳纳米管的层与层之间靠 结合在一起。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为 。
(3)用价层电子对互斥理论推断SnBr2分子中Sn—Br的键角 120°(填“>”“<”或“=”)。
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为 ,每个Ba2+与 个O2-配位。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016浙江宁波效实中学高二上期中考试化学试卷卷(解析版) 题型:选择题
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g),ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、容器体积的关系如下表所示:
nY(g),ΔH=Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、容器体积的关系如下表所示:
温度 | 1 | 2 | 4 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20[ | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是
A.m>n
B.温度不变,压强增大,Y的质量分数减少
C.Q<0
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源:2016届山东省青岛市高三上学期期中测试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中,一定能大量共存的是
A.与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42-
B.在0.1 mol·L-1Na2CO3溶液中:A13+、Na+、NO3-、C1-
C.水电离的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、AlO2-、CO32-
D.在c(H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源:2016届新疆兵团农二师华山中学高三上学期第二次月考化学试卷(解析版) 题型:选择题
某合作学习小组讨论辨析:
①漂白粉和酸雨都是混合物;
②煤和石油都是可再生能源;
③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
④不锈钢和目前流通的硬币都是合金:
⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;⑥豆浆和雾都是胶体。
上述说法正确的是
A.①②④⑤ B.①②⑤⑥ C.①③④⑥ D.②③④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上学期期中测试化学试卷(解析版) 题型:填空题
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
实验编号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的 pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | c | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸___________________________。
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________(选填“是”或“否”),混合液中离子浓度c(A-)与 c(Na+)的大小关系是________________________。
(3)丙组实验结果分析,HA是________酸(选填“强”或“弱”),该混合溶液中离子浓度由大到小的顺序是____________________。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol·L-1。
写出该混合溶液中下列算式的精确结果(不能做近似计算)。
c(Na+)-c(A-)=________mol·L-1 , c(OH-)-c(HA)=________mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上学期11月月考化学试卷(解析版) 题型:填空题
NaCl是一种化工原料,可以生产一系列物质(见下图)。

(1)25℃,NaHCO3在水中的溶解度比Na2CO3的_____(填“大”、“小”或“不能确定”)
(2)已知氯化钠在25℃的溶解度为36g,则该温度下饱和氯化钠的质量分数为______(计算结果保留一位小数)。
(3)碳酸氢钠受热分解的化学方程式是_______
(4)用氯气生产氯化氢的化学方程式是________
(5)食盐水通电后发生反应的离子方程式是_______
查看答案和解析>>
科目:高中化学 来源:2016届北京市海淀区高三上学期期中测试化学试卷(解析版) 题型:选择题
右图是元素周期表的一部分,下列关系判断正确的是
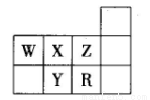
A.原子半径:Y > X > W
B.氢化物的沸点:W > X > Y
C.氢化物的稳定性:R > Y > X
D.简单阴离子的还原性:Y > R > Z
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江哈尔滨附属中学高二上期中化学试卷(解析版) 题型:简答题
将1.2mol的A气体充入2L恒容密闭容器中发生反应:A(g)  2B(g)。在三种不同条件下进行实验,A的物质的量随时间的变化如图所示。试回答下列问题:
2B(g)。在三种不同条件下进行实验,A的物质的量随时间的变化如图所示。试回答下列问题:
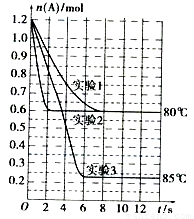
(1)实验1中,4s时A的转化率为 ;此条件下该反应的平衡常数K1的值为 。
(2)实验2与实验1对比,其可能隐含的反应条件是 。
(3)根据实验3与实验1的图象比较,可推测该反应是 (填“放热”或“吸热”)反应。设实验1~3的平衡常数的值分别为K1、K2、K3,则它们之间的关系为K1 K2 K3(填“>”、“<”或“=”)。
(4)为了验证增大催化剂的表面积、增大压强可提高化学反应速率这一结论,某同学在实验1的基础上又利用该容器设计了实验4和实验5,部分实验条件及数据见下表。请将表格补充完整。
实验编号 及其目的 | V(容积)/L | t/℃ | n(A起始)/mol | n(B起始)/mol | 催化剂的质量/g | 催化剂的表面积/m2·g—1 |
实验1参照对比实验 | 2 | 80 | 1.2 | 0 | a | b |
实验4:催化剂的表面积对反应速率的影响 | ||||||
实验5目的: | 1 |
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
①NaCl的摩尔质量是58.5g
②在C与SiO2反应制备SiC中,氧化剂与还原剂的物质的量之比是2:1
③标准状况下,1 L HCl和1 L H2O的物质的量相同
④标准状况下,1 g H2和16 g O2的体积相同
⑤摩尔质量就等于物质的式量
⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑦在同温同体积时,气体物质的物质的量越大,则压强越大
⑧同温同压下,气体的密度与气体的相对分子质量成正比
A.①②③④ B.②③⑥⑦⑧ C.⑤⑥⑦⑧ D .④⑦⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com