
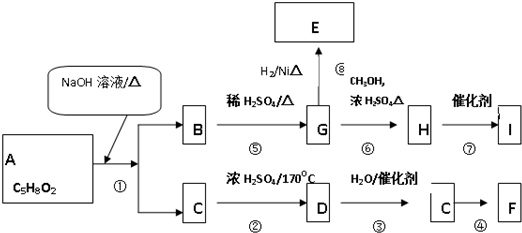
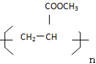
���� ����I�ṹ��ʽ֪��H�����Ӿ۷�Ӧ����I��HΪCH2=CHCOOCH3��G����������Ӧ����H����GΪCH2=CHCOOH��G�����ӳɷ�Ӧ����E��EΪCH3CH2COOH��
A�ܷ���ˮ�ⷴӦ����B��C��B�����ữ�õ�G����BΪCH2=CHCOONa��
����A����ʽ��A��ֻ��һ����֪��A�ṹ��ʽΪCH2=CHCOOCH2CH3��C���Ҵ����ṹ��ʽΪCH3CH2OH��C������ȥ��Ӧ����D��DΪCH2=CH2����ϩ��ˮ�����ӳɷ�Ӧ�����Ҵ���F�ܷ���������Ӧ��˵��F�к���ȩ������C����������Ӧ����F����FΪCH3CHO���ݴ˷������
��� �⣺����I�ṹ��ʽ֪��H�����Ӿ۷�Ӧ����I��HΪCH2=CHCOOCH3��G����������Ӧ����H����GΪCH2=CHCOOH��G�����ӳɷ�Ӧ����E��EΪCH3CH2COOH��A�ܷ���ˮ�ⷴӦ����B��C��B�����ữ�õ�G����BΪCH2=CHCOONa��
����A����ʽ��A��ֻ��һ����֪��A�ṹ��ʽΪCH2=CHCOOCH2CH3��C���Ҵ����ṹ��ʽΪCH3CH2OH��C������ȥ��Ӧ����D��DΪCH2=CH2����ϩ��ˮ�����ӳɷ�Ӧ�����Ҵ���F�ܷ���������Ӧ��˵��F�к���ȩ������C����������Ӧ����F����FΪCH3CHO��
��1��AΪCH2=CHCOOCH2CH3��A�к��еĹ����ţ�̼̼˫�����������ʴ�Ϊ��̼̼˫����������
��2��ͨ�����Ϸ���֪������ȡ����Ӧ���У��٢ޣ��ʴ�Ϊ���٢ޣ�
��3����Ӧ�ܵĻ�ѧ����ʽΪ2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
�ʴ�Ϊ��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
��4��A�Ľṹ��ʽΪCH2=CHCOOCH2CH3���ʴ�Ϊ��CH2=CHCOOCH2CH3��
��5��E�DZ��ᣬE�ж���ͬ���칹�壬����һ�ּ��ܷ���������Ӧ���ܺ�NaOH��Һ��Ӧ����������к���������ȩ����ΪHCOOCH2CH3��
�ʴ�Ϊ��HCOOCH2CH3��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬��I�ṹ��ʽΪͻ�ƿڲ�������˼ά�����жϣ����ؿ���ѧ�������ƶ�������ע���Ϸ�Ӧ�����ƶϣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
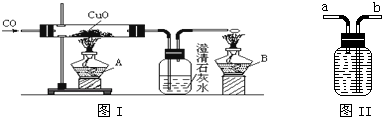
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
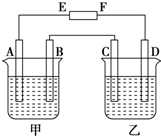 ��ͼ�У�E��F�ֱ�Ϊ��Դ���������ձ���ʢ��100mL 0.2mol•L-1 AgNO3��Һ�����ձ���ʢ��100mL 0.15mol•L-1 CuCl2��Һ��A��B��C��D��Ϊʯī�缫��������һ��ʱ�����B������1.08g����
��ͼ�У�E��F�ֱ�Ϊ��Դ���������ձ���ʢ��100mL 0.2mol•L-1 AgNO3��Һ�����ձ���ʢ��100mL 0.15mol•L-1 CuCl2��Һ��A��B��C��D��Ϊʯī�缫��������һ��ʱ�����B������1.08g�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ܱ������г���1 mol N2��3 mol H2����ַ�Ӧ������NH3�ķ�����ĿΪ2NA | |
| B�� | ��״���£�44.8 L���������Ĺ��õ��Ӷ���ĿΪ2NA | |
| C�� | ���³�ѹ�£�1 mol NaHSO4�����к��е�������ĿΪ2NA | |
| D�� | 1 mol Fe��71 g Cl2��ַ�Ӧ��ת�Ƶĵ�����ĿΪ3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Na2O2�м�������ˮ��2Na2O2+2H2O=4Na++4OH-+O2�� | |
| B�� | ��Ag��NH3��2NO3��Һ�м������Ag��NH3��2++2H+=Ag++2NH4+ | |
| C�� | ��Al2��SO4��3��Һ�м��������ˮ��Al3++3OH-=Al��OH��3�� | |
| D�� | ��Ca��HCO3��2��Һ�м������ʯ��ˮ��Ca2++2HCO3-+2OH-=CaCO3��+CO32-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
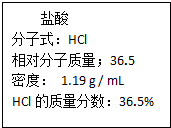 ��I�����Т١�������Na��Mg��H��O��S��Cl��Ԫ���еļ�����ɣ��������ʵ���ɺ����ʽ����ǽ����˷��࣮
��I�����Т١�������Na��Mg��H��O��S��Cl��Ԫ���еļ�����ɣ��������ʵ���ɺ����ʽ����ǽ����˷��࣮| ������� | ����ǿ�� | �� | ���� |
| ��ѧʽ | ��H2SO4��HClO4 | �� ��Mg��OH��2 ��Mg��OH��2 | ��NaCl ��Na2SO3 |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
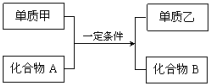 �û���Ӧ��ͨʽ�ɱ�ʾΪ��
�û���Ӧ��ͨʽ�ɱ�ʾΪ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com