
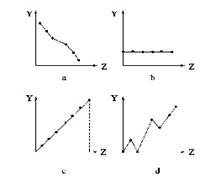
(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:
①ⅡA族元素的价电子数____________。
②第三周期元素的最高化合价__________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y元素原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。
据此回答:①N的最高价氧化物对应的水化物的化学式为________ 。
②工业上制取单质M的化学方程式为_____________________________________。
③用电子式表示ZN及X2Y的形成化合物的过程————————————————————————————————————;———————————————————————————————————————————————————————————————————— 。
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
| 弱酸 | CH3COOH | H2SO3 | HCN |
| 物质的量浓度mol/L | 0.01 | 0.01 | 0.01 |
| pH | 3.4 | 2.3 | 5.6 |
 HSO3-+OH-
HSO3-+OH- HSO3-+OH-
HSO3-+OH-| c(H+) |
| c(CH3COOH) |
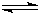 H+(aq)+CN-(aq)△H=+43.5kJ?mol-1
H+(aq)+CN-(aq)△H=+43.5kJ?mol-1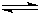 HCN(aq)+OH-(aq)的△H=
HCN(aq)+OH-(aq)的△H=查看答案和解析>>
科目:高中化学 来源: 题型:
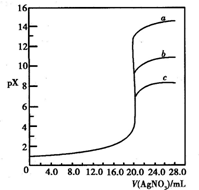 用0.1mol?L-1?AgNO3溶液分别滴定20.00mL含Cl-、Br-、I-浓度均为0.1mol?L-1的溶液,以滴入的AgNO3溶液的体积为横坐标,pX为纵坐标[pX=-lg c(X),X=Cl-、Br-、I-],可得如图所示的滴定曲线.已知25℃时,部分难溶盐的Ksp和颜色如表所示: 用0.1mol?L-1?AgNO3溶液分别滴定20.00mL含Cl-、Br-、I-浓度均为0.1mol?L-1的溶液,以滴入的AgNO3溶液的体积为横坐标,pX为纵坐标[pX=-lg c(X),X=Cl-、Br-、I-],可得如图所示的滴定曲线.已知25℃时,部分难溶盐的Ksp和颜色如表所示:
|
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省南昌二中高二上学期期末考试化学试卷 题型:填空题
(8分)室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(0C)
随加入盐酸体积变化曲线如右图所示。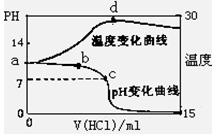
(1)下列有关说法正确的是___________
A.a点由水电离出的C(H+)=10-14mol/L
B.b点:
C.c点:C(Cl-)=C(NH4+)
D.d点后,容易温度略下降的主要原因是NH3·H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先 后 (填“增大”、“减小”或“不变”);
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和
溶液的pH。试填写表中空白:
| | 离子浓度的关系 | 溶质 | 溶液的pH | 物料守恒关系 |
| ① | C(NH4+)>C(Cl-)>C(OH-)>C(H+) | | pH>7 | / |
| ② | | NH4Cl | / | |
| ③ | C(Cl-)>C(H+)>C(NH4+)>C(OH-) | | pH<7 | / |
查看答案和解析>>
科目:高中化学 来源:2013届江西省高二上学期期末考试化学试卷 题型:填空题
(8分)室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(0C)
随加入盐酸体积变化曲线如右图所示。

(1)下列有关说法正确的是___________
A.a点由水电离出的C(H+)=10-14mol/L
B.b点:
C.c点:C(Cl-)=C(NH4+)
D.d点后,容易温度略下降的主要原因是NH3·H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先 后 (填“增大”、“减小”或“不变”);
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和
溶液的pH。试填写表中空白:
|
|
离子浓度的关系 |
溶质 |
溶液的pH |
物料守恒关系 |
|
① |
C(NH4+)>C(Cl-)>C(OH-)>C(H+) |
|
pH>7 |
/ |
|
② |
|
NH4Cl |
/ |
|
|
③ |
C(Cl-)>C(H+)>C(NH4+)>C(OH-) |
|
pH<7 |
/ |
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com