
分析 根据氧气的体积可求得氧气的物质的量,设需要的KClO3的物质的量为xmol,根据反应可求出X,然后即可求出所需氯酸钾的质量,然后根据即可求出所需纯度为95%的氯酸钾质量,据此计算.
解答 解:由于氧气在标况下的体积为4.48L,故氧气的物质的量n=$\frac{4.48L}{22.4L/mol}$=0.2mol,设需要的KClO3的物质的量为xmol,根据反应可知:
2KClO3 $\frac{\underline{\;加热\;}}{\;}$2KCl+3O2↑
2 3
xmol 0.2mol
故有:$\frac{2}{xmol}=\frac{3}{0.2mol}$
解得X=$\frac{4}{30}$mol
故所需的纯氯酸钾的质量m=nNA=$\frac{4}{30}mol$×122.5g/mol=16.3g,
故所需纯度为95%的氯酸钾质量m=$\frac{16.3g}{95%}$=17.2g.
答:所需的纯度为95%的氯酸钾质量为17.2g.
点评 本题考查了根据化学方程式所进行的有关计算,难度不大,应注意基础的掌握.


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该饱和溶液的物质的量浓度为5.07mol•L-1 | |
| B. | 向该溶液中加入等体积的水之后溶液的质量分数小于13.25% | |
| C. | 25℃时,密度等于1.12g•cm-3的NaCl溶液是饱和溶液 | |
| D. | 将此溶液蒸发掉部分水,再恢复到20℃时,溶液密度一定大于1.12g•cm-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$
CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$ CHCl-CH3(g)+HCl(g)△H>0
CHCl-CH3(g)+HCl(g)△H>0| 时间/(min) | 0 | 2 | 5 | 6 | 9 | 10 |
| χ(乙苯) | 0.5 | 0.25 | 0.1 | 0.1 | 0.05 | 0.05 |
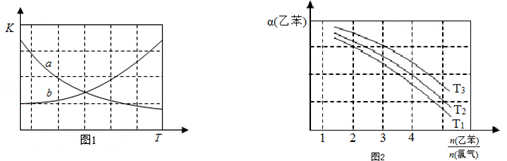
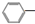 CH2CH3(g)$\stackrel{催化剂}{?}$
CH2CH3(g)$\stackrel{催化剂}{?}$ CH=CH2(g)+H2(g)△H=+124kJ/mol
CH=CH2(g)+H2(g)△H=+124kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验探究 | 实验操作及现象 | 结论分析 |
| 探究一 | 将淡蓝绿色粉末溶解于盐酸溶液中,取上清液2份, ①1份滴加BaCl2溶液,产生白色沉淀,再加盐酸,无明显变化. ②另1份溶液先滴加KSCN溶液,无明显变化,再滴加双氧水,后滴加KSCN溶液溶液,变成血红色. | 证明淡蓝绿色粉末为FeSO4 |
| 探究二 | 将红色物质研成粉末,滴加盐酸,无明显变化,再滴加KSCN溶液,无明显现象. | 证明:红色物质不是Fe2O3. |

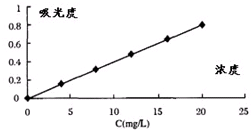
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
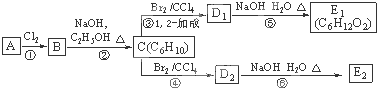
 ;
;
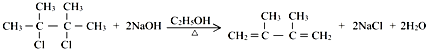 ;
; +Br2→
+Br2→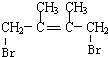 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com