
碘酸钾是一种白色结晶粉末,无臭无味,酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、二氧化硫等还原性物质作用,被还原为单质碘,在碱性介质中,碘酸钾能被氯气、次氯酸盐等氧化为高碘酸钾。碘酸钾在常温下稳定,加热至560℃开始分解。工业生产碘酸钾的流程如下,在反应器中发生反应的化学方程式为:I2+KClO3+H2O--KH(IO3)2+KCl+Cl2 ↑(未配平)
(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同,请配平该反应的化学方程式:______________________________________________________________;
(2)步骤②中,用稀酸酸化的作用是____________________________________________;
不选稀盐酸的原因是 ;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为 ;
(4)参照下表碘酸钾的溶解度,步骤11得到碘酸钾晶体,你建议的方法是 。
| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
(1)6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑ (2分)
(2)促进氯气从反应混合物中逸出。(2分)盐酸能还原已生成的碘酸氢钾(2分)
(3)Cl2能将KIO3氧化成KIO4 (2分) (4)蒸发浓缩 冷却结晶 (2分)
解析试题分析:(1)反应I2→KH(IO3)2中,I元素化合价由0价升高为+5价,共升高10价。KClO3→KCl、Cl2,氯元素化合价降低,还原产物为KCl、Cl2。KClO3→KCl氯元素化合价由+5降低为-1价,化合价降低6价,KClO3→Cl2氯元素化合价由+5降低为0价,化合价总共降低10价,二者获得的电子数目相同,获得电子最小公倍数为30,则KCl的系数为5,Cl2的系数为3,所以化合价降低共60价,故I2系数为6,根据氯原子守恒可知KClO3系数为11,根据碘原子守恒可知KH(IO3)2的系数为6,根据氢原子守恒可知H2O、系数为3,检查氧原子守恒,故方程式为6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑。(2)由信息可知,碘酸钾能被氯气氧化,由工艺流程可知酸化的目的是将氯气从反应混合物中逸出。酸性条件下碘酸钾是一种较强的氧化剂,盐酸能还原已生成的碘酸氢钾,所以不能使用稀盐酸。
(3)由信息可知,碘酸钾能被氯气氧化为高碘酸钾,所以要将氯气完全排出,防止碘酸钾被氧化。
(4)由表中数据可知温度越高,KIO3溶解度越大,所以从溶液中获得KIO3晶体的实验方法是蒸发浓缩、 冷却结晶。
考点:考查物质制备的实验设计与探究以及氧化还原反应的有关判断和方程式的配平


 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案科目:高中化学 来源: 题型:填空题
金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2=4CuSO4+ 2H2O,该反应的还原剂是 ,当1mol O2发生反应时,还原剂所失电子的物质的量为 mol。向CuSO4溶液中加入镁条时有气体生成,该气体是
(3)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为
(4)某化学小组在实验中用浓硝酸和铜反应制取二氧化氮并探究二氧化氮是否能支持木炭的燃烧,其实验装置图如下:
①按气流方向连接各仪器接口,顺序为a→______→______→______→______→f。
②已知二氧化氮和碳反应生成两种物质的量比为1:1的有毒气体,则该反应的化学方程式为:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O反应中。
(1) 元素被氧化,氧化产物是 ; 还原产物是 ;氧化剂和还原剂的物质的量之比为
(2)用双线桥法表示该反应的电子转移情况。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知盐酸参加的下列三个反应:
① CaCO3+2HCl=CaCl2+CO2↑+H2O
② Fe+2HCl=FeCl2+H2↑
③ MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)判断上述三个反应中属于氧化还原反应的是_________,其中盐酸作还原剂的是__________。
(2)上述反应说明盐酸具有_______性,______性,_______性。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
向盛有KI溶液的试管中加入少许CC14后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CC14层会逐渐变浅,最后变成无色。完成下列填空:
(1)上述过程CCl4层在试管中位于 (填上、下)层,分离CC14层和水层的操作名称是____ ,使用的玻璃仪器是 。
(2)写出并配平CC14层由紫色变成无色的化学反应方程式(如果系数是l不用填写);
+ + → HIO3+
(3)把KI换成KBr。则CC14层变为 色,该反应的离子方程式为 。继续滴加氯水,CCl4层的颜色没有变化。Cl2、 HIO3、HBrO3氧化性由强到弱的顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知硫氰(SCN)2为拟卤素,其分子及阴离子的性质与卤素性质相似。完成下列填空:将硫氰化钾溶液与氯化铁溶液混合,溶液变为血红色。
(1)写出该反应的化学方程式 。
将生成的血红色溶液分为四等份,进行如下实验(第四份是对照):
(2)第一份中加入少量的氯化钾固体,溶液的颜色 (填“会”或“不会”)加深。
(3)第二份中滴加入碘化钾溶液至过量,再加入四氯化碳,充分振荡,最终水层接近无色,四氯化碳层呈 色,写出该过程的离子方程式
。
向该溶液中滴加少量溴水,水溶液又变为血红色,则氧化性Br2 (SCN)2(填“大于”、“小于”或“无法确定”)。
(4)第三份中加入少量酸性高锰酸钾溶液,血红色褪去。完成并配平该反应的离子方程式。若含 mol高锰酸钾的溶液完全反应,转移电子2mol。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
硝酸盐受热分解的产物与硝酸盐的组成以及受热的温度等因素有关。
Ⅰ.一定条件下硝酸铵受热分解的化学反应方程式为:NH4NO3→HNO3+N2 +H2O(未配平)
(1)该反应中发生还原反应的过程是_______→________。
(2)反应中被氧化与被还原的氮原子数之比为__________;现有1mol NH4NO3分解,生成的氧化产物的物质的量是 mol。
Ⅱ.硝酸铵受撞击或高温发生爆炸的化学反应方程式为:m NH4NO3→n O2+p N2+q H2O
(3)下列关于该方程式中化学计量数的说法正确的是_________(选填字母编号)。
a.m=1 b.n=2 c.p=3 d.q=4
(4)若反应过程中共转移3.01×1023个电子,则反应可产生气体的体积为_____(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
为了防止枪支生锈,常将枪支的钢铁零件放在NaNO2和NaOH的混合液中进行化学处理使钢铁零件表面生成Fe3O4的致密的保护层——“发蓝”。其过程可用下列化学方程式表示:
①3Fe NaNO2
NaNO2 5NaOH → 3Na2FeO2
5NaOH → 3Na2FeO2 H2O
H2O NH3↑
NH3↑
② Na2FeO2 NaNO2
NaNO2 H2O → Na2Fe2O4
H2O → Na2Fe2O4 NH3↑
NH3↑ NaOH
NaOH
③Na2FeO2 Na2Fe2O4
Na2Fe2O4 2H2O
2H2O Fe3O4
Fe3O4 4NaOH
4NaOH
(1)配平化学方程式②。
(2)上述反应①中还原剂为 ,被还原的是 。若有1mol Na2FeO2生成,则反应中有 mol电子转移。
(3)关于形成“发蓝”的过程,下列说法正确的是…………………………………………( )
| A.该生产过程不会产生污染 | B.反应③生成的四氧化三铁具有抗腐蚀作用 |
| C.反应①②③均是氧化还原反应 | D.反应①②中的氧化剂均为NaNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学兴趣小组在探究卤素单质的氧化性的实验中发现,在足量的氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色,原因是什么?Br2能否氧化Fe2+,Fe3+与Br2谁的氧化性更强?
(1)甲同学认为:Br2不能氧化Fe2+,Fe3+的氧化性大于Br2,产生上述现象的原因不是化学反应所致,溶液呈黄色是含 (填化学式,下同)所致。
(2)乙同学认为:Br2将Fe2+氧化为Fe3+,Fe3+的氧化性小于Br2,产生上述现象的原因是化学反应所致,则溶液呈黄色是含 所致。
(3)丙同学为验证乙同学的观点,选择下列试剂,设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点是正确的,供选用的试剂:a.酚酞试剂;b.CCl4;c.无水酒精;d.KSCN溶液。请你在下表中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
| 选用试剂 | 实验现象 |
| 方案1 | |
| 方案2 | |
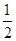 的Br-被氧化成单质Br2,则原FeBr2溶液的物质的量浓度是 。
的Br-被氧化成单质Br2,则原FeBr2溶液的物质的量浓度是 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com