
����Ŀ��ij��ȤС���Ʊ�����������������
ʵ��1 |
| ʵ������ |
Һ���Ϸ�������ɫ��״������Ѹ�ٱ�Ϊ����ɫ�����Թܱ����к��ɫ�������ɡ� |
(1)ʵ��1�в�����ɫ���������ӷ���ʽ��_______��
(2)Ϊ��̽�����������ɫ��ԭ��С��ͬѧչ������̽����
�ټ�ͬѧ�Ʋ����ɫ����ΪFe(OH)2��Fe(OH)3�����������Ϻ���ݵ�ɫԭ����Ϊ��ɫ�ͺ��ɫ�ĵ���ɫ�������ǻ���ɫ�������ʵ��֤ʵ����ɫ�����в�����Fe(OH)3��������______��
����ͬѧ�������ף�Fe(OH)2�ڴ���SO42-���ڵ�������γ�Fe6(SO4)2(OH)4O3(һ�ֻ���ɫ������ʽ����)������ƶԱ�ʵ��֤ʵ�ü��裺���Թ��м���________�������Թ��м���_________����������ʵ��1��ͬ�������Ǹü��費������
����ͬѧ�����������ף�Fe(OH)2�������н�ǿ���������ܣ�����ɫ��������Fe(OH)2��������Fe2+�����Ʋ����õ�����������Һ��Ũ��ӦԽСԽ�ã�����������ҺŨ��ӦԽ��Խ�á����������ʵ�鷽����
�Թ���10mLNaOH��Һ | �μ�FeSO4��Һ | ʵ������ | |
ʵ��2 | 6 mol/LNaOH��Һ | 0.2mol/L FeSO4��Һ | ����������Һ��İ�ɫ����(������������ɫ)�������³��ֻ���ɫ��Ϊ��ɫ���� |
ʵ��3 | 6 mol/LNaOH��Һ | 0.1mol/L FeSO4��Һ | ����������Һ��İ�ɫ����(���м���������ɫ)�������³��ײ���Ϊ��ɫ���� |
��ʵ��ó��Ľ�����________����ͬѧ��Ϊ��ʵ�鷽��������֤������ɫ����Fe(OH)2��������Fe2+����ģ����貹���ʵ����__________��֤���ü��������
(3)��������ʵ��̽�������������Ƶð�ɫFe(OH)2��������Ҫ���Ƶ�ʵ������_____��
(4)��������ᵼ������NaOH��Һ��Ũ��ƫ�ߵ���_______��
A.NaOH��Һδ��ȴ�����¾ͽ��ж��� B.����ǰ����ƿ����������ˮ
C.������Һʱ����������ƿ�̶��� D.��ˮʱ�����̶��ߣ��ý�ͷ�ι�����
���𰸡�Fe2++2OH-=Fe(OH)2�� ȡһ�����Ļ���ɫ���������������ܽ⣬�ټ���KSCN��Һ������Һ�����ɫ����֤������ɫ�����в�����Fe(OH)3 2mL 0.1mol/LFeCl2��Һ 3��0.1mol/L NaOH��Һ ������������ҺŨ��һ���������£�����������Һ��Ũ��ԽС��������ɫ����������Խ���� ��ʵ��2(��ʵ��3)�İ�ɫ�����м����������������������Һ����ɫ������ɻ���ɫ ���������������������������������ƹ���������������Ũ��С������������Ũ�ȴ� AC
��������
(1)FeSO4��NaOH��Һ�������ֽⷴӦ����Fe(OH)2��ɫ������
(2)�ٽ�����ɫ�����������ܽ⣬Ȼ�����Fe3+�����ʣ���SCN-���飻
�ڸ���ʵ��һ������
�۲��öԱ�ʵ�飬���ݿ��Ʊ�����������
(3)����Fe2+���ױ����������ʵ��1��2��3�Ľ��۷������
(4)����c=![]() �������ʵ���Ũ����Һ������
�������ʵ���Ũ����Һ������
(1)FeSO4��NaOH��Һ�������ֽⷴӦ����Fe(OH)2��ɫ��������Ӧ�����ӷ���Ϊ��Fe2++2OH-=Fe(OH)2����
(2)��Fe(OH)3��������ˮ������ᷴӦ���������Ե����Σ������Һ�м���KSCN��Һ������Һ�����ɫ����֤������ɫ�����в�����Fe(OH)3��
�����Թ��м���2mL0.1mol/LFeCl2��Һ�������Թ��м���3��0.1mol/L NaOH��Һ����������ʵ��1��ͬ�������Ǹü��費������
�۸���ʵ��2��3��֪����NaOHŨ����ͬʱ������������Һ��Ũ��ԽС��������ɫ����������Խ���ԣ���ͬѧ��Ϊ��ʵ�鷽��������֤������ɫ����Fe(OH)2��������Fe2+����ģ����貹���ʵ������ʵ��2(��ʵ��3)�İ�ɫ�����м����������������������Һ����ɫ������ɻ���ɫ��֤���ü��������
(3)����Fe2+���ױ������е���������������Ҫ�����ܸ������������ʵ��1��2��3�Ľ���Ҫʹ������������(���������ƹ���)����������Ũ��С(����������Ũ�ȴ�)�ȴ�ʩ�ſ����Ƶð�ɫFe(OH)2������
(4) A.NaOH��Һδ��ȴ�����¾ͽ��ж��ݣ�����Һ�ָ�������ʱ����Һ��Һ����ڿ̶��ߣ���Һ�����ƫС������������ҺŨ��ƫ�ߣ�A�������⣻
B.����ǰ����ƿ����������ˮ�����ڲ�Ӱ�����ʺ���Һ���������˶����Ƶ���ҺŨ����Ӱ�죬B���������⣻
C.������Һʱ����������ƿ�̶��ߣ���Һ�����ƫС���������Ƶ���ҺŨ��ƫ�ߣ�C�������⣻
D.��ˮʱ�����̶��ߣ��ý�ͷ�ι���������Һ�����ƫ�������Ƶ���ҺŨ��ƫ�ͣ�D���������⣻
�ʺ���ѡ����AC��


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��Ϊ̽��Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�顣
��.��1�����ơ��ء�þ������1 mol�ֱ�Ͷ�뵽������0.1 mol��L��1�������У���Ԥ��ʵ������__________�����ᷴӦ����ң�__________�����ᷴӦ������
��2����NaOH��Һ��NH4Cl��Һ�������NH3��H2O���Ӷ���֤NaOH�ļ��Դ���NH3��H2O���̶�������֤Na�Ľ����Դ���N������Ϊ������Ƿ��������˵�����ɣ�_______,________________��
��.������ͼװ�ÿ�����֤�ǽ����Եı仯���ɡ�

��3������A������Ϊ________�������D��������_____________________________��
��4��ʵ����������ҩƷNa2S��KMnO4��Ũ���ᡢMnO2����ѡ�����ҩƷ���ʵ����֤�ȵķǽ����Դ�����װ��A��B��C����װҩƷ�ֱ�Ϊ________��________��________��װ��C�е�ʵ������Ϊ�е���ɫ�������ɣ����ӷ���ʽΪ_________________________��
��5����Ҫ֤���ǽ����ԣ�C>Si����A�м�________��B�м�Na2CO3��C�м�________���۲쵽C����Һ������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�з�Ӧ�����Ʊ�SiH4��һ�ַ������丱����MgCl2��6NH3�����ʵ�þ��Դ���ش��������⣺

��1��MgCl2��6NH3����Ԫ�صļ����Ӱ뾶��С�����˳��H-���⣩��_________________________��Mg��Ԫ�����ڱ��е�λ�ã�_____________________��Mg(OH)2�ĵ���ʽ��____________________��
��2��A2B�Ļ�ѧʽΪ_______________����Ӧ�ڵıر�������_______________����ͼ�п���ѭ��ʹ�õ�������_______________��
��3����һ�������£���SiH4��CH4��Ӧ����H2��һ�ֹ�����ĥ����_______________��д��ѧʽ����
��4��Ϊʵ��ȼú������ú�м��뽬״Mg(OH)2��ʹȼ�ղ�����SO2ת��Ϊ�ȶ���Mg�����д���÷�Ӧ�Ļ�ѧ����ʽ��_______________��
��5����Mg�Ƴɵĸ����Լ���RMgBr���������л��ϳɣ������Ʊ��������ĺϳ�·�����£�
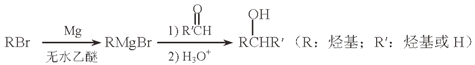
����������Ϣ��д���Ʊ�![]() ����ȩ�Ŀ��ܽṹ��ʽ��_______________��
����ȩ�Ŀ��ܽṹ��ʽ��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ũ�Ⱦ�Ϊ3mol��L��1��H2SO4��NaOH��Һ��100 mL�У��ֱ��������������ۣ���Ӧ��Ϻ����������������Ϊ4��5����������۵����ʵ���Ϊ�� ��
A.0.125molB.0.25molC.0.5molD.1mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������γɶ��ֻ������Fe��SCN��3��[Fe��CO��5]���ʻ������������������������й㷺Ӧ�á�
��1��Fe3+��̬��������Ų�ʽΪ_____��
��2��ʵ������KSCN��Һ��������Һ����Fe3+��N��O��S�ĵ�һ�������ɴ�С��˳��Ϊ____����SCN���е�̼ԭ�ӵ��ӻ��������Ϊ_____����SCN����Ϊ�ȵ�����ķ�����_____��
��3���ʻ���[Fe��CO��5]������������1mol[Fe��CO��5]�����к�������ĿΪ_____��
��4��ij�ֵ����������ľ�����ͼ��ʾ���õ���������Ļ�ѧʽΪ_____��
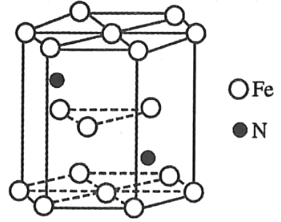
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ת���ڸ��������²���ʵ�ֵ���
A. NH3![]() NO
NO![]() HNO3
HNO3
B. Ũ����![]() Cl2
Cl2![]() Ư��
Ư��
C. Al2O3![]() AlCl3(aq)
AlCl3(aq)![]() ��ˮAlCl3
��ˮAlCl3
D. ������![]() C2H5OH
C2H5OH![]() CH3CHO
CH3CHO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��COCl2�����������������ж����塣��һ�������£��ɷ����Ļ�ѧ��ӦΪ��COCl2(g) ![]() CO(g)��Cl2(g)����H<0 �����й�˵������ȷ����
CO(g)��Cl2(g)����H<0 �����й�˵������ȷ����
A. ��һ�������£�ʹ�ô����ܼӿ췴Ӧ����
B. ����Ӧ��ƽ��ʱ�����º�ѹ������ͨ��Ar��COCl2��ת���ʲ���
C. ��λʱ��������CO������Cl2�����ʵ�����Ϊ1��1ʱ����Ӧ�ﵽƽ��״̬
D. ƽ��ʱ�������������䣬�����¶ȿ�ʹ�÷�Ӧ��ƽ�ⳣ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ƽ������[KNH4Fex(SO4)y(OH)z]������ˮ��ϡ���ᣬ��ȡ�Ƽ��������ʾ��ͼ���£�
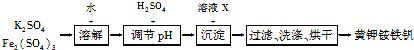
��1����ҺX��________��
��2��������Һ���Ƿ����K���IJ�����________________________��
��3���Ƽ�������Ļ�ѧʽ��ͨ������ʵ��ⶨ��
����ȡһ����������Ʒ����ϡ�������ܽ⣬��������Һת��������ƿ�����Ƴ�100.00 mL��ҺA��
����ȡ25.00 mL��ҺA�����������ữ��BaCl2��Һ��������ȫ�����ˡ�ϴ�ӡ����������أ��õ���ɫ����9.32 g��
����ȡ25.00 mL��ҺA����������NaOH��Һ�����ȣ��ռ�����״��������224 mL��ͬʱ�к��ɫ�������ɡ�
�������������ó������ˡ�ϴ�ӡ����գ����յù���4.80 g����Ƽ�������Ļ�ѧʽΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ǹ���һ�ֻ�ѧƷ����ѧʽCr(OH)������غ�ɫ������һ���Ʊ����������ڷ����ϵ�����ý���п����ԭ���������۸���ԭΪ���۸������۸���������������Һ���ü����Ƶ��������Ǹ���ʵ��װ����ͼ��ʾ���ش��������⣺
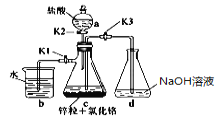
��֪����1��Cr(OH)�����ʺ�Fe(OH)���ƣ��Ʊ���ʱ��Ҫ�ϸ��������
��2��Cr3�� ��ɫ��Cr2������ɫ
��1��ʵ������������ˮ��Ҫ������ԭ����_______________________�����跽����__________��
����a��������____________��
��2��������п�����Ȼ�����������c�У�������������ˮ����ͼ���Ӻ�װ�á���K1��K2���ر�K3����c����Һ����ɫ�ѱ�Ϊ����ɫ���÷�Ӧ�����ӷ���ʽΪ��____________________��
��ͬʱc���������������������______________ ����������____________��
��3����K3���ر�K1��K2��c������ɫ��Һ����d�У���ԭ����______________________��
��4��ָ��dװ�ÿ��ܴ��ڵ�ȱ��_____________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com