
发射卫星时可用肼(N2H4)为燃料和二氧化氮做氧化剂,两者反应生成氮气和气态水.
已知;N2(g)+2O2(g)=2NO2(g)△H=67.7kJ•mol﹣1
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣543kJ•mol﹣1
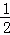 H2(g)+
H2(g)+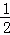 F2(g)=HF(g)△H=﹣269kJ•mol﹣1
F2(g)=HF(g)△H=﹣269kJ•mol﹣1
H2(g)+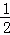 O2(g)=H2O(g)△H=﹣242kJ•mol﹣1
O2(g)=H2O(g)△H=﹣242kJ•mol﹣1
(1)肼和二氧化氮反应的热化学方程式为
(2)有人认为若用氟代替二氧化氮作氧化剂,则反应释放能量更大,肼和氟反应的热化学方程式为 .
考点:
热化学方程式.
专题:
化学反应中的能量变化.
分析:
(1)依据热化学方程式和盖斯定律计算得到;
(2)依据热化学方程式,结合目标热化学方程式,利用盖斯定律计算得到;
解答:
解:(1)①N2(g)+2O2(g)=2NO2(g)△H=67.7kJ•mol﹣1
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣543kJ•mol﹣1
依据盖斯定律②×2﹣①得到,2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=﹣1153.7kJ•mol﹣1;
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=﹣1153.7kJ•mol﹣1 ;
(2)①N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣543kJ•mol﹣1
②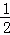 H2(g)+
H2(g)+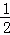 F2(g)=HF(g)△H=﹣269kJ•mol﹣1
F2(g)=HF(g)△H=﹣269kJ•mol﹣1
③H2(g)+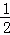 O2(g)=H2O(g)△H=﹣242kJ•mol﹣1
O2(g)=H2O(g)△H=﹣242kJ•mol﹣1
依据盖斯定律①﹣③×2+②×4得到:N2H4(g)+2F2(g)=N2(g)+4HF (g)△H=﹣1135kJ•mol﹣1;
故答案为:N2H4(g)+2F2(g)=N2(g)+4HF (g)△H=﹣1135kJ•mol﹣1;
点评:
本题考查了热化学方程式的计算和盖斯定律的计算应用,理解实质,掌握基础是解题关键,题目较简单.


科目:高中化学 来源: 题型:
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | Na2S有强还原性 | 用于除去废水中的Cu2+和Hg2+ |
| B | CaCO3是难溶物 | CaCl2溶液中通入CO2产生白色沉淀 |
| C | 浓H2SO4有强氧化性 | 浓H2SO4可用于干燥SO2 |
| D | Zn具有还原性和导电性 | 可用作锌锰干电池的负极材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图:利用Fe+CuSO4=FeSO4+Cu反应设计一个原电池.下列说法中,正确的是( )
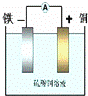
|
| A. | 电解质溶液中阳离子向负极移动 |
|
| B. | 电子通过溶液由负极流向正极 |
|
| C. | 当导线中有1mol电子通过时,理论上正极消耗28克. |
|
| D. | 若所选电极的质量相等,理论上两极质量差为60g,导线中有1mol电子通过 |
查看答案和解析>>
科目:高中化学 来源: 题型:
向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2.在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g.下列有关说法不正确的是( )
|
| A. | Cu与Cu2O的物质的量之比为2:1 |
|
| B. | 硝酸的物质的量浓度为2.6mol/L |
|
| C. | 产生的NO在标准状况下的体积为4.48L |
|
| D. | Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )

|
| A. | 任何化学反应都伴随着能量的变化 |
|
| B. | H2O(g)═H2O(l)该过程放出大量的热,所以该过程是化学变化 |
|
| C. | 化学反应中能量的变化都表现为热量的变化 |
|
| D. | 对于如图所示的过程,是吸收能量的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一固定体积的密闭容器中,充入2mol A和1mol B,发生如下反应:2A(g)+B(g)═xC(g),平衡后,C的体积分数为W%,若维持容器容积和温度不变,0.6mol A、0.3mol B 和1.4mol C为起始物质,达到平衡后,C的体积分数也为W%.平衡后若缩小容器体积,C的浓度c(C)、C的体积分数C%、混合气体平均相对分子质量(M)和正反应速率,随压强(P)的变化,一定符合的是( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
对可逆反应4NH3(g)+5O2(g)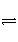
 4NO(g)+6H2O(g),下列叙述正确的是( ) A.达到化学平衡时,4v正(O2)=5v逆(NO)
4NO(g)+6H2O(g),下列叙述正确的是( ) A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成xmolNO的同时消耗xmolNH3,则反应达到平衡状态
C.化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v正(H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com