
(ԭ��) �ο���Ϣ��6��14�ձ�������ý�ƣ��й���������������Ϊ����ĺ��շ��������·���������Ӧ���ߵ��ڲ��¶ȣ�ӵ�и���ɫ�����ܻ������ԣ��ܿ��ܱ���װ����ս�ɻ��ϣ�������й�����ʦ������������������蝹����Ͻ�ҶƬ�ļ�����������ԭ�����³�Ʒ�����ʣ������Ʊ����������Ϸ��֣��(Re)���۵�3180�棬�е�5627�棻��������������õĻ�е���ܣ���Ȼ����2���ԭ��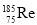 ��
�� ������˵������ȷ����
������˵������ȷ����
A��������蝹����Ͻ����ڽ�������
B�� ��
�� ��������
��������
C���(Re)Ԫ�ص����ԭ������Ϊ186
D����諸Ͻ�ȴ�蝹��۵�ߡ�Ӳ�ȴ�
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014��������У����5�µ���������Կ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��CH4����ԭNOx�������������������Ⱦ����֪��
��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) ��H=��574 kJ/mol
��CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H=��1160 kJ/mol
��H2O(g)=H2O(l) ��H=��44kJ/mol������˵������ȷ����
A�������ʵ�����CH4�μӷ�Ӧ����Ӧ�٢�ת�Ƶĵ�������ͬ
B��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H=��530 kJ/mol
C��0.2 mol CH4��ԭNO2��N2��������H2O(g)�ų�������Ϊ164.6 kJ
D������4.48 L(��״��)CH4��ԭNO2��N2������H2O(g)������������ת�Ƶ���1.60 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����һ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��15�֣�������ֲ��֦Ҷ��ȡ�ľ����к������мס������ֳɷ֣�
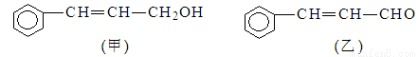
��1���������������ŵ�����Ϊ ��
��2���ɼ�ת��Ϊ���辭���й��̣�����ȥ������Ӧ���ز����ͬ����
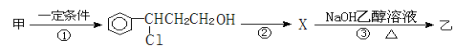
��Ʋ���ٵ�Ŀ���� ��ָ���ٵķ�Ӧ���� ��
��Ӧ�ڵĻ�ѧ����ʽΪ ��ע����Ӧ��������
��3�����������еĺ��������ţ�ѡ�����е�һ���Լ���__________��
A����ˮ B�����Ը��������Һ C�����CCl4��Һ D��������Һ
��4���Ҿ����⻯�������õ�����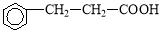 ����д��ͬʱ��������Ҫ��ı���ͬ���칹��ṹ��ʽ__________________��_________________
����д��ͬʱ��������Ҫ��ı���ͬ���칹��ṹ��ʽ__________________��_________________
���ܷ���������Ӧ��������FeCl3��Һ������ɫ��Ӧ���ۺ˴Ź�������ͼ�ϲ���4�����շ塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����һ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪�з�Ӧ��I2��g����H2��g�� 2HI��g����H��0���÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ��x��ֵ����y��x�仯���ƺ�������
2HI��g����H��0���÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ��x��ֵ����y��x�仯���ƺ�������
ѡ�� | X | Y |
|
A | �¶� | �����ڻ��������ܶ� | |
B | I2�����ʵ��� | H2��ת���� | |
C | H2��Ũ�� | ƽ�ⳣ��K | |
D | ����Ar�����ʵ��� | �淴Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����һ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ԭ������NA��ʾ�����ӵ�������ֵ������������ȷ����
A����״���£�46g NO2�к��еķ�����ΪNA
B��ͨ��״���£�14g CO���еĵ�����ĿΪ7NA
C��1L 0.2 mol/L��CH3COOH��Һ�У�H+ ��ĿΪ0.2NA
D��0.1mol Cu ����40mL 10mol/L���ᷴӦ����Һ�е�NO3����ĿΪ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и���˫�����Ի�ѧ�Ծ��������棩 ���ͣ������
��ѡ��3-���ʵĽṹ�����ʡ���15�֣�

�ϱ�Ϊ���ڱ���һ���֣����еı�Ŵ�������Ӧ��Ԫ�ء���ش��������⣺
��1�����Ԫ�صĻ�̬ԭ�ӵļ۵����Ų�ʽ��________������ͬ���ڣ��һ�̬ԭ�ӵĺ���δ�ɶԵ���������Ԫ����______(д��Ԫ�ط���)���ں�Ԫ�ػ�̬ԭ�ӵĵ����Ų�ͼΪ___��
��2�� �ٺ���ۺ�Ԫ���γɵĺ���18���ӵ�����Ϊ________(д������)���ں���ۺ�Ԫ���γɵģ����������ЧӦ�����ʵĿռ乹��Ϊ________��
�ڡ��ܡ�������Ԫ�ص�ԭ���γɵľ��壬�侧���Ľṹ�ص���ͼ��ʾ����û�����Ļ�ѧʽΪ________(�ö�Ӧ��Ԫ�ط��ű�ʾ)�����������±�ϩ����̬������Է��������ȱ�ϩС�ļ״�������������ȴ��Һ̬���������������ԭ����____________��

��3���١�������Ԫ�����γɶ���ƽ���η��ӣ�������һ����Է���������С���йظ÷��ӵ�˵������ȷ����________��
a���÷������ں��м��Լ��ķǼ��Է���b���÷��Ӻ���4���Ҽ���1���м�
c���÷����еĢ�ԭ�Ӳ�ȡsp2�ӻ�d��������������ˮ�����ܺ�ˮ��Ӧ�õ��ƾ�
��4��ijԪ�صļ۵����Ų�ʽΪnsnnpn��1����Ԫ�ؿ���Ԫ�آ��γɺ���10�����ӵķ���X����������Xͨ��ʢ������ͭ��Һ���Թ������������Ϊ_______��
��5�� ��DԪ����FeԪ���γ�ij�־�����ͼ��ʾ���������ı߳�Ϊa nm����Ͻ���ܶ�Ϊ________g/cm3��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и���˫�����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ����Fe��Fe2O3��������2 mol��L-1��HNO3��Һ25mL�У���Ӧ��ɺ�����ʣ�࣬����224mLNO���壨��״����������Ӧ�����Һ�м���1 mol��L-1��NaOH��Һ��Ҫʹ��Ԫ��ȫ����������������NaOH��Һ�����������
A��45mL B��50mL C��40mL D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ�����и���˫�����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ�Ѿ�������������ĸ������棬����˵������ȷ����
A��2011��3��11�գ��ձ���������𣬲������˵糧��ը���˷�Ӧ���������仯
B�����⻯ѧ���������������ն��������������ꡱ���γɶ��뵪���������й�
C����̼����ע�ؽ��ܼ��ţ�����ʹ��̫���ܵȴ��滯ʯȼ�ϣ���������������ŷ�
D���ߴ��ȵĹ赥�ʹ㷺�����������ά�����ά��ǿ��ᡰ��·��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014���������б�ҵ���Ͽ������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣�������һ�̵ֹ��ķ�����1100��CͨN2��CaC2��Ӧ�õ�CaCN2 ��
��֪��CaCN2+3H2O = 2NH3+CaCO3 ��CaC2+2H2O = C2H2��+Ca(OH)2


��1��ijͬѧ��������װ�ã����Ⱥͼг���������ȥ����ȡ������CaCN2
��U�ι���ʢ�ŵ������� ����һ�֣���
�� (��ܡ����ܡ�)����ͨ�����ܴ���ͼ��ʯӢ�ܣ�
��2�����鷴Ӧ��Ĺ��壨��W��ʾ���к��е�Ԫ�ظ�ͬѧ������W����ˮ�������ݲ�����˵�������к��е�Ԫ�أ��ý��۲���ȷ����Ҫ�ó���ȷ���ۣ�������е�ʵ���� ��
��3���ⶨW��CaCN2����������
�������ͼ��ʾװ�ã��г���������ȥ������ʵ�飺�رյ��ɼУ���©������Һ��μ��뵽����ƿ�У���W��Ӧ��ȫ���ɼУ�ͨ�뵪����ֱ��������200mL0.1 mol��L-1������ȫ���ա�
�����ȷ��ȡ�ձ�����Һ20.00mL������ƿ�У����뼸��ָʾ������cmol��L-1NaOH��Һ�ζ����������ᣬʵ�������ı���Һ��ƽ�����ΪvmL��
��֪���ֳ���ָʾ����ɫpH��Χ���£�
ָʾ�� | a | b | c |
��ɫpH��Χ | 3.1��4.4 | 8.0��10.0 | 4.4��6.2 |
˵�� | pH��3.1�Ժ�ɫ pH��4.4�Ի�ɫ | pH��8.0����ɫ pH��10.0�Ժ�ɫ | pH��4.4�Ժ�ɫ pH��6.2�Ի�ɫ |
�������ζ������У�����ѡ�õ�ָʾ���� ������ĸ��ţ���
���ձ����������հ��������ʵ���Ϊ mol������һ����������W��CaCN2����������
������ʵ�����ý������ƫС����������װ�õ������ԺͲ��������½��ƫС�Ŀ���ԭ����
��д1�֣���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com