
【题目】填空题
(1)KHSO4溶液的pH______(填“>”“<”或“=”)7,用离子方程式表示为___________。
(2)KHCO3溶液的pH_____(填“>”“<”或“=”)7,用离子方程式表示为____________。
(3)将上述两种溶液混合,现象是_______________,用离子方程式表示为___________。
【答案】< KHSO4===K++H++SO![]() > HCO
> HCO![]() +H2O==H2CO3+OH- 产生气泡 H++HCO
+H2O==H2CO3+OH- 产生气泡 H++HCO![]() ===H2O+CO2↑
===H2O+CO2↑
【解析】
(1)硫酸氢钾溶液中电离出氢离子,溶液显酸性,据此分析;
(2)碳酸氢钾溶液中存在碳酸氢根离子的水解和电离,水解程度大于电离程度,溶液显碱性,据此分析;
(3)二者混合,反应生成二氧化碳和水,据此分析。
(1).硫酸氢钾电离出氢离子,溶液显酸性,pH <7 ,电离方程式为:KHSO4===K++H++SO![]() ;
;
(2) 碳酸氢钾溶液中存在碳酸氢根离子的水解和电离,水解程度大于电离程度,溶液显碱性,pH>7,水解的离子方程式为:HCO![]() +H2O==H2CO3+OH-;
+H2O==H2CO3+OH-;
(3).硫酸氢钾和碳酸氢钾反应生成硫酸钾和水和二氧化碳,现象为:产生气泡,反应的离子方程式为:H++HCO![]() ===H2O+CO2↑。
===H2O+CO2↑。


科目:高中化学 来源: 题型:
【题目】Ⅰ:用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________。
(2)如果按图中所示的装置进行试验,求得的中和热数值_______(填“偏大、偏小、无影响”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与(2)中实验相比,所求中和热_________ (填“相等”或“不相等”)。
Ⅱ: (1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6),丙烷脱氢可得丙烯。已知:C3H8(g) === CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6 kJ·mol-1
CH3CH=CH2(g)=== CH4(g)+ HC≡CH(g ) △H2=+32.4 kJ·mol-1
则C3H8(g) === CH3CH=CH2(g)+H2(g) △H =______________ kJ·mol-1。
(2)发射火箭时用肼(N2H4)作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知32gN2H4(g)完全发生上述反应放出568kJ的热量,热化学方程式是:____________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于难溶盐MX,其饱和溶液中M+和X-浓度之间的关系为Ksp=c(M+)c(X-),现将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的顺序是( )
①20mL0.01molL-1KCl溶液;②30mL0.02molL-1CaCl2溶液;③40mL0.03molL-1HCl溶液;④10mL蒸馏水;⑤50mL0.05molL-1AgNO3溶液
A.①>②>③>④>⑤B.④>①>③>②>⑤
C.⑤>④>②>①>③D.④>③>⑤>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4-溴环己烯(![]() )可与下列4种物质发生反应:①HBr、②酸性高锰酸钾溶液、③氢氧化钠的水溶液、④氢氧化钠的乙醇溶液。下列有关这些反应的说法中正确的是( )
)可与下列4种物质发生反应:①HBr、②酸性高锰酸钾溶液、③氢氧化钠的水溶液、④氢氧化钠的乙醇溶液。下列有关这些反应的说法中正确的是( )
A.与①反应后的有机产物只有一种
B.与②的反应原理类似于烯烃使溴水褪色
C.与③反应后得到的有机产物可被氧化为醛
D.与④反应后得到的有机产物只有一种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A. 氮原子的价电子排布图:![]()
B. 2p和3p轨道形状均为哑铃形,能量也相等
C. 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
D. 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究燃料的燃烧和对污染气体产物的无害化处理,对于防止大气污染有重要意义。
(1)将煤转化为清洁气体燃料。
已知:2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol;
C(s)+O2(g)=CO(g) △H=-110.5kJ/mol
写出焦炭与水蒸气反应制H2和CO的热化学方程式_________。
(2)已知一定温度和压强下,由H2和CO反应合成优质燃料甲醇:
CO(g)+2H2(g)![]() CH3OH(g) △H=-91kJ/mol
CH3OH(g) △H=-91kJ/mol
①在相同条件下要想得到182kJ热量,加入各物质的物质的量可能是________
A.2molCO和4molH2 B.2molCO、1molCH3OH和4molH2
C.4molCO和4molH2 D.4molCO和6molH2
②将1molCO和2molH2充入一密闭容器中,保持恒温恒压时进行反应,达到平衡时,测得CO的转化率为20%,若在相同条件下,起始时在该容器中充入CH3OH(g),反应达到平衡时的热量变化是______(填“吸收”或“放出”)_______kJ热量。
Ⅱ.在1.0L恒容密闭容器中放入0.10molA(g),在一定温度进行如下反应。
A(g)![]() 2B(g)+C(g)+D(s) △H=+85.5kJ/mol
2B(g)+C(g)+D(s) △H=+85.5kJ/mol
容器内气体总压强(p)与起始压强p0的比值随反应时间(t)变化数据见下表(提示:密闭容器中的压强比等于气体物质的量之比)。

回答下列问题:
(3)下列能提高A的转化率的是___。
A.升高温度 B.向体系中通入A气体
C.减少D的物质的量 D.向体系中通入稀有气体He
(4)相同条件下,若该反应从逆向开始,建立与上述相同的化学平衡,则D的取值范围_________。
(5)将容器改为恒压容器,改变条件,使反应达到相同的限度,则达到平衡时B的浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式为( )
A.浓盐酸与铁屑反应:2Fe+6H+=2 Fe3++3H2↑
B.钠与 CuSO4 溶液反应: 2Na + Cu2+ = Cu 2Na
C.足量Na2CO3溶液中清入几滴稀H2SO4 :![]() + 2H+ = H2O + CO2
+ 2H+ = H2O + CO2
D.向 FeCl3 溶液中加入铜粉: Cu + 2Fe3+ = 2Fe2+ + Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各电离方程式中,书写正确的是( )
A.CH3COOH![]() H++CH3COO-
H++CH3COO-
B.KHSO4![]() K++H++ SO42-
K++H++ SO42-
C.Al(OH)3![]() Al3++3OH-
Al3++3OH-
D.H2CO3![]() 2H++ CO32-
2H++ CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的分子式为C5H12Cl,用NaOH的醇溶液处理X,可得到分子式为C5H10的两种产物Y、Z。Y、Z经催化加氢后都可得到2-甲基丁烷.则X的结构简式可能为( )
A.![]() B.
B.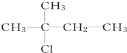
C.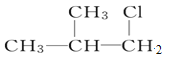 D.
D.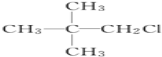
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com