
| A | B | C | D | |
| 研究目的 | 压强对反应的影响 | 温度对反应的影响 | 增加O2浓度对反应的影响 | 浓度对平衡常数的影响 |
| 图示 | 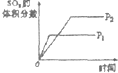 |  | 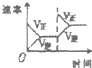 |  |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| A、2C8H18(l)+25O2(g)═16CO2(g)+18H2O(l);△H=-11036kJ/mol | ||
B、C(s)+
| ||
C、H2(g)+
| ||
D、CO(g)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、50mL 18.4mol?L-1浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
| B、常温常压下,4.6gNO2与N2O4混合气中含有0.3NA个原子 |
| C、1L0.1mol?L-1Na2CO3溶液中含有的阴离子数为0.1NA |
| D、标准状况下,22.4LCCl4中含有NA个分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
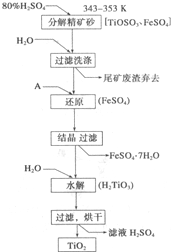 钛白粉(主要成分是Ti02),覆盖能力强,折射率高,无毒,广泛用于油漆、塑料、造纸等行业,还可用作乙醇脱水、脱氢的催化剂.如图是以钛铁矿(主要成分FeTi03,钛酸亚铁)为主要原料生产钛白粉的工艺流程图,回答下列问题:
钛白粉(主要成分是Ti02),覆盖能力强,折射率高,无毒,广泛用于油漆、塑料、造纸等行业,还可用作乙醇脱水、脱氢的催化剂.如图是以钛铁矿(主要成分FeTi03,钛酸亚铁)为主要原料生产钛白粉的工艺流程图,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

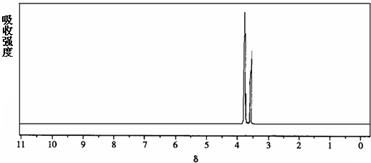
查看答案和解析>>
科目:高中化学 来源: 题型:
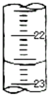 实验室用中和滴定法测定待测烧碱溶液的浓度,试根据实验回答:
实验室用中和滴定法测定待测烧碱溶液的浓度,试根据实验回答:| 滴定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
| 第三次 | 10.00 | 4.20 | 25.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:
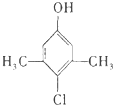 某品牌的家用消毒剂其有效成分为对氯间二甲苯酚(结构简式如图所示),可以杀灭常见的病毒与细菌.下面有关该物质的说法正确的是( )
某品牌的家用消毒剂其有效成分为对氯间二甲苯酚(结构简式如图所示),可以杀灭常见的病毒与细菌.下面有关该物质的说法正确的是( )| A、该物质的分子式是C8H10Cl |
| B、1mol该物质最多可以与2mol氢氧化钠反应 |
| C、1mol该物质可以与2molBr2发生取代反应 |
| D、该物质可以发生加成、取代、消去、氧化等反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com