
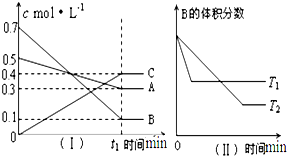
 T��ʱ��A������B���巴Ӧ����C���壮��Ӧ������A��B��CŨ�ȱ仯��ͼ������ʾ�������������������䣬�¶ȷֱ�ΪT1���T2��ʱ��B�����������ʱ��Ĺ�ϵ��ͼ������ʾ�������н��۲���ȷ���ǣ�������
T��ʱ��A������B���巴Ӧ����C���壮��Ӧ������A��B��CŨ�ȱ仯��ͼ������ʾ�������������������䣬�¶ȷֱ�ΪT1���T2��ʱ��B�����������ʱ��Ĺ�ϵ��ͼ������ʾ�������н��۲���ȷ���ǣ�������| A����t1ʱ������B��ʾ�÷�Ӧ��ƽ������Ϊ0.6/t1mol?L-1?min-1 | B���÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ��A+3B?2C | C�������������䣬����ѹǿ�������淴Ӧ���ʾ����������ƽ����Է����������� | D�������������䣬�¶���T1���ߵ�T2��ƽ��ʱB��ת���ʽ��� |
| 0.6mol/L |
| t1min |
| 0.6 |
| t1 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 T��ʱ����һ�����Ϊ2L�������У�A������B���巴Ӧ����C���壬��Ӧ������A��B��CŨ�ȱ仯��ͼ��ʾ��
T��ʱ����һ�����Ϊ2L�������У�A������B���巴Ӧ����C���壬��Ӧ������A��B��CŨ�ȱ仯��ͼ��ʾ�� C
C C
C�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
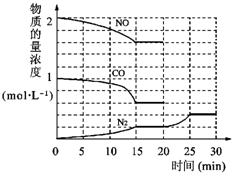 �������ⱸ�������ע���������Լ�����β���ŷŵ�һ����̼��CO�����������NOx������������强��Ϊ������Ⱦ����Ҫ���أ�
�������ⱸ�������ע���������Լ�����β���ŷŵ�һ����̼��CO�����������NOx������������强��Ϊ������Ⱦ����Ҫ���أ� O2+Hb?CO
O2+Hb?CO N2��g��+2CO2��g����H=-113kJ?mol-1
N2��g��+2CO2��g����H=-113kJ?mol-1| 0.4 |
| 15 |
| 0.4 |
| 15 |
 H2��g��+CO2��g����ƽ�ⳣ�����¶ȵı仯���±���
H2��g��+CO2��g����ƽ�ⳣ�����¶ȵı仯���±���| �¶�/�� | 400 | 500 | 830 | 1000 |
| ƽ�ⳣ��K | 10 | 9 | 1 | 0.6 |
| A | B | C | D | |
| n��CO2�� | 3 | 1 | 0 | 1 |
| n��H2�� | 2 | 1 | 0 | 1 |
| n��CO�� | 1 | 2 | 3 | 0.5 |
| n��H2O�� | 5 | 2 | 3 | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
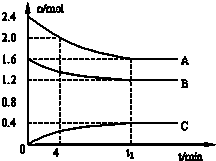
��1��ij�¶��£��ܱ������У��������¿��淴Ӧ��2E��g��![]() F(g) + xG��g��, ��H��0������ʼʱE��Ũ��Ϊa mol/L��F ,GŨ�Ⱦ�Ϊ0����ƽ��ʱEŨ��Ϊ0.5a mol/L ;��E����ʼŨ�ȸ�Ϊ2a mol/L��F ,GŨ����Ϊ0�����ﵽ��ƽ��ʱ��
F(g) + xG��g��, ��H��0������ʼʱE��Ũ��Ϊa mol/L��F ,GŨ�Ⱦ�Ϊ0����ƽ��ʱEŨ��Ϊ0.5a mol/L ;��E����ʼŨ�ȸ�Ϊ2a mol/L��F ,GŨ����Ϊ0�����ﵽ��ƽ��ʱ��
����X=1,����������ֲ��䣬��ƽ����E���������Ϊ________.
����X=2������������ֲ��䣬��ƽ����F��ƽ��Ũ��____0.5a mol/L��
��2��t�潫3mol A�����1mol B����ͨ��2L�̶�������ܱ������У��������·�Ӧ��3A(g) + B��g��![]() xC��g����2minʱ��Ӧ�ﵽƽ��״̬���¶Ȳ��䣩��ʣ����0.8molB�������C��Ũ��Ϊ0.4mol/L������д����հף�
xC��g����2minʱ��Ӧ�ﵽƽ��״̬���¶Ȳ��䣩��ʣ����0.8molB�������C��Ũ��Ϊ0.4mol/L������д����հף�
�ٴӿ�ʼ��Ӧ���ﵽƽ��״̬������C��ƽ����Ӧ����Ϊ_________,X=_____.
����������ԭƽ��������ͨ�����������������뷴Ӧ����ѧƽ�⽫____�ƶ���
������ԭƽ��������������ٳ���a molC����t��ﵽ�µ�ƽ�⣬��ʱB�����ʵ���Ϊn��B��=_____________mol��
�����������Ӧ����ͬ�¶Ⱥ������н��У���ʹ��Ӧ�ﵽƽ��ʱ���ʵ���������ԭƽ��ʱ��ͬ����ʼ������������ʵ����ʵ���n��A��n(B) n(C)֮��Ӧ������Ĺ�ϵΪ_____________________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ���㽭ʡ������ʮУ�߶����£����л�ѧ�Ծ��������棩 ���ͣ������

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com