
分析 2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价由+7价降低为+2价,Cl元素的化合价由-1价升高为0,16molHCl中10molHCl作还原剂,以此来解答.
解答 解:①2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价降低,被还原,则氧化剂为KMnO4,
故答案为:KMnO4;Mn;
②标准状况下若有2.24L Cl2生成,n(Cl2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O~被氧化的10HCl~10电子
5 10 10
0.1mol x y,
则x=0.21mol,y=0.2mol,所以电子转移的数目为0.2mol×NA=0.2NA,
故答案为:0.2mol;0.2NA.
点评 本题考查氧化还原反应,为高频考点,把握发生的氧化还原反应及元素的化合价变化为解答的关键,注意从元素化合价角度分析,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ①>②>③ | B. | ②>①>③ | C. | ②>③>① | D. | ③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(s)+O2(g)═SO2(g)△H=-296.8 kJ/mol(反应热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3 kJ/mol(中和热) | |
| C. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1 367.0 kJ/mol(燃烧热) | |
| D. | 2NO2═O2+2NO△H=+116.2 kJ/mol(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
A、利用该装置准确量取9.20ml硫酸溶液 | B、将洗涤液转移到容量瓶中,应该采取如图的操作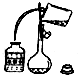 |
| C、过滤和蒸发中都需要使用玻璃棒,且玻璃棒的用途一样 | D、保存NaOH应使用带橡皮塞的玻璃试剂瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2能与金属活动性顺序表中大多数金属发生化学反应 | |
| B. | N2是大气的主要成分之一,雷雨时,可直接转化为NO2 | |
| C. | 硫是一种淡黄色的能溶于水的晶体,只有氧化性 | |
| D. | 某气体通入澄清石灰水有白色沉淀产生,该气体一定是CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
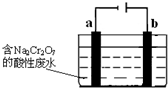 工业上可用电解法来处理含Cr2O72-的酸性废水,最终可将Cr2O72-转化成Cr(OH)3沉淀而被除去.如图为电解装置示意图(电极材料分别为铁和石墨):
工业上可用电解法来处理含Cr2O72-的酸性废水,最终可将Cr2O72-转化成Cr(OH)3沉淀而被除去.如图为电解装置示意图(电极材料分别为铁和石墨):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com