
| A、Y的化学式为Fe2O3 |
| B、S4O62-是还原产物 |
| C、被1mol O2氧化的Fe2+物质的量为1mol |
| D、每 32 gO2参加反应,转移电子的物质的量为4mol |


科目:高中化学 来源: 题型:

| 物质类别 | 强酸 | 强碱 | 正盐 | 氧化物 | 氢化物 |
| 化 学 式 |
①HCl ② |
③ ④Ba(OH)2 |
⑤Na2CO3 ⑥ |
⑦CO2 ⑧Na2O |
⑨NH3 ⑩H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属Na、Mg、A1熔、沸点由高到低 |
| B、HC1、HBr、HI的还原性由强到弱 |
| C、H+、Li+、H- 的半径由小到大 |
| D、同浓度的硫酸钠、醋酸钠、碳酸钠溶液的碱性由强到弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlO2-+2H2O?Al(OH)3+OH- |
| B、HCO3-+H2O?H3O++CO32- |
| C、HCO3-+OH-═CO32-+H2O |
| D、NH3+H2O?OH-+NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔融状态下的NaHSO4电离:NaHSO4═Na++H++SO42- |
| B、H2CO3的电离:H2CO3?2H++CO32- |
| C、Fe(OH)3的电离:Fe(OH)3?Fe3++3OH- |
| D、Na2CO3的水解:CO32-+2H2O?H2CO3+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-=BaSO4↓ |
| B、稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| D、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
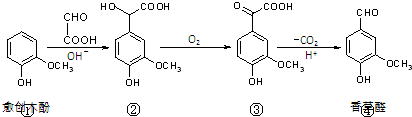 ( )
( )| A、在上述三步反应中理论上只有①生成②的反应原子利用率为100% |
| B、氯化铁溶液和碳酸氢钠溶液都能鉴别③④ |
| C、②分子中C原子不可能在同一平面上 |
| D、等物质的量的①②分别与足量NaOH溶液反应,消耗NaOH的物质的量之比为1:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com