
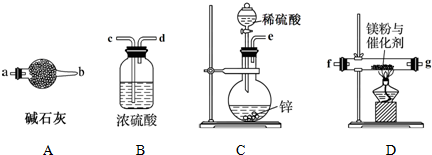
分析 (1)制备LiH固体需要制备氢气和锂发生反应,LiH在干燥的空气中能稳定存在,遇水或酸能够引起燃烧,所以制备得到的氢气必须干燥纯净,利用C装置制备氢气,用这种A中的碱石灰除去氢气中的氯化氢和水蒸气,通入装置D中加热和锂反应生成氢化锂,最后连接装置B防止空气中的水蒸气和二氧化碳进入装置D和生成的氢化锂发生反应;
(2)有气体参加加热或燃烧的反应需要首先验纯,实验完毕后先熄火、冷却,再停止气体生成,防止倒吸发生爆炸;
(3)用无水硫酸铜可以检验气体中是否含有水;
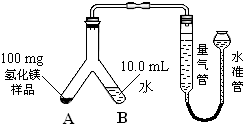
(4))①读取量气管中数据时,为减小误差,应使水准管、量气管内液面相平;
②反应生成氢气的体积为量气管中两次液面刻度的差值;
③根据m=ρV可计算出氢气的质量,根据方程式MgH2+2H2O=Mg(OH)2↓+2H2↑可计算出氢化镁的质量,进而确定样品中氢化镁的纯度;
(5)镁粉与氧气反应生成 氧化镁,而氢化镁与氧气反应能生成水,根据是否有水产生鉴别镁粉与氢化镁.
解答 解:(1)制备LiH固体需要制备氢气和锂发生反应,LiH在干燥的空气中能稳定存在,遇水或酸能够引起燃烧,所以制备得到的氢气必须干燥纯净,利用C装置制备氢气,用这种A中的碱石灰除去氢气中的氯化氢和水蒸气,通入装置D中加热和锂反应生成氢化锂,最后连接装置B防止空气中的水蒸气和二氧化碳进入装置D和生成的氢化锂发生反应,装置连接顺序为:e接a,b接f,g接c,
故答案为:eabfgc;
(2)有气体参加加热或燃烧的反应需要首先验纯,实验完毕后先熄火、冷却,再停止气体生成,防止倒吸发生爆炸,故正确的操作顺序为②③④①,
故答案为:②③④①;
(3)用无水硫酸铜可以检验气体中是否含有水,所以可在D装置前面再加一个装置,该装置中加入无水硫酸铜,
故答案为:无水硫酸铜;
(4)①读取量气管中数据时,为减小误差,应使水准管、量气管内液面相平,
故答案为:抬高(或移动)水准管位置,使水准管、量气管内液面相平;
②反应生成氢气的体积为量气管中两次液面刻度的差值,所以氢气的体积为128.0mL-10.0mL=118.0mL,
故答案为:118.0;
③根据m=ρV可计算出氢气的质量为0.09mg/mL×118.0mL=10.62mg,根据方程式MgH2+2H2O=Mg(OH)2↓+2H2↑可知氢化镁的质量为$\frac{26}{4}×10.62$mg=69.03mg,所以样品中氢化镁的纯度为$\frac{69.03mg}{100mg}$×100%=69.03%,
故答案为:69.03%;
(5)镁粉与氧气反应生成 氧化镁,而氢化镁与氧气反应能生成水,根据是否有水产生鉴别镁粉与氢化镁,实验方法为:分别取适量的固体粉末,在加热的条件下与干燥的氧气反应,将产生的气体通过装有无水硫酸铜的干燥管,若观察到白色固体变蓝,则固体样品为MgH2,若白色固体没有变蓝,则固体样品为镁粉,
故答案为:分别取适量的固体粉末,在加热的条件下与干燥的氧气反应,将产生的气体通过装有无水硫酸铜的干燥管,若观察到白色固体变蓝,则固体样品为MgH2,若白色固体没有变蓝,则固体样品为镁粉.
点评 本题考查了物质组成的实验探究方法和流程分析判断,实验装置的连接顺序和分析判断,化学方程式定量计算的应用,掌握基础是关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 第一步 | B. | 第二步 | C. | 第三步 | D. | 第四步 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 相对分 子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醇 | |||||
| 1-萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
| 1-乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
| 乙醇 | 46 | 无色液体 | -114.1℃ | 78.5℃ | 任意比混溶 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
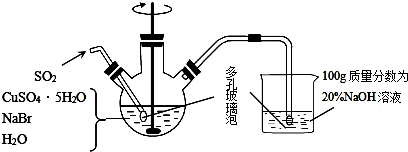
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
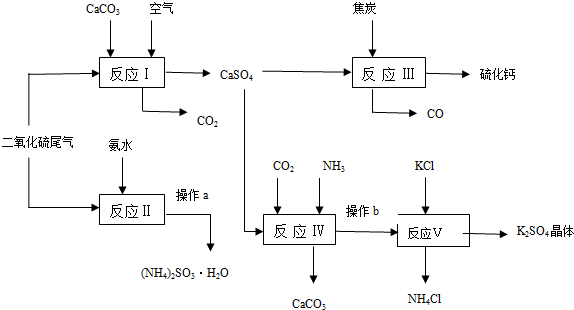
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制饭勺、高压锅等的不锈钢是纯铁 | B. | 铝制品可以长期用作餐具 | ||
| C. | Al(OH)3可用于制胃酸中和剂 | D. | 医用酒精浓度是95% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com