
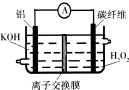
| A.铝作负极,电池工作时将不断溶解 |
| B.该电池不是二次电池,不可充电 |
| C.碳纤维电极的电极反应是H202+2e-+2H+=2H2O |
| D.电池工作时OH-从碳纤维电极透过离子交换膜移向Al电极 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
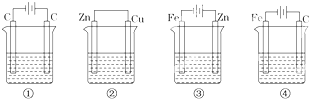
| A.由Fe、Cu与稀硫酸溶液组成的原电池,其负极反应式为:Fe-3e-═Fe3+ |
| B.由Al、Mg与氢氧化钠溶液组成的原电池,其负极反应式为:Mg-2e-+2OH-═Mg(OH)2 |
| C.由Pb、Cu与氯化铁溶液组成的原电池,其正极反应式为:Cu-2e-═Cu2+ |
| D.由Al、Cu与浓硝酸组成的原电池,其负极反应式为:Cu-2e-═Cu2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
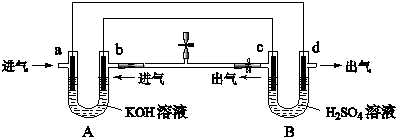
| A.装置A是原电池,装置B是电解池 |
| B.反应一段时间后,装置B中溶液PH增大 |
| C.a口若消耗1molCH4,d口可产生4mol气体 |
| D.a口通入C2H6时的电极反应为C2H6-14e-+18OH-═2CO32-+12H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2Al+WO3
| ||||
B.2Ag2O
| ||||
C.3CO+Fe2O3
| ||||
D.2AlCl3(熔融)
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
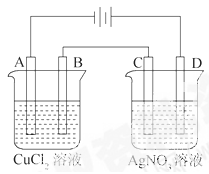
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com