
【题目】某药物H的合成路线如下:

试回答下列问题:
(1)反应Ⅰ所涉及的物质均为烃,氢的质量分数均相同。则A分子中最多有______个原子在同一平面上,最多有______个碳原子在同一条直线上。
(2)反应Ⅰ的反应类型是______反应Ⅱ的反应类型是______,反应Ⅲ的反应类型是______。
(3)B的结构简式是______;E的分子式为______;F中含氧官能团的名称是___。
【答案】16 3 加成反应 取代反应 消去反应 ![]() C10H12O2 醛基、酯基
C10H12O2 醛基、酯基
【解析】
根据合成线路可以知道,D与新制Cu(OH)2加热条件下反应,酸化后得苯乙酸,则D的结构简式为:![]() ;C催化氧化生成D,则C的结构简式为:
;C催化氧化生成D,则C的结构简式为:![]() ;B水解生成C,则B的结构简式为:
;B水解生成C,则B的结构简式为:![]() ;A与溴化氢在双氧水的作用下发生加成反应生成B,所以A为
;A与溴化氢在双氧水的作用下发生加成反应生成B,所以A为![]() ,反应Ⅰ所涉及的物质均为烃,氢的质量分数均相同,比较苯与A的结构可以知道,苯与X发生加成反应生成A,所以X为CH≡CH;苯乙酸与乙醇在浓硫酸作用下发生酯化反应生成E为
,反应Ⅰ所涉及的物质均为烃,氢的质量分数均相同,比较苯与A的结构可以知道,苯与X发生加成反应生成A,所以X为CH≡CH;苯乙酸与乙醇在浓硫酸作用下发生酯化反应生成E为![]() ,E发生取代反应生成F,F与氢气发生加成,醛基转化为羟基,则G的结构简式为:
,E发生取代反应生成F,F与氢气发生加成,醛基转化为羟基,则G的结构简式为:![]() ,G发生消去反应生成H;据以上分析解答。
,G发生消去反应生成H;据以上分析解答。
根据合成线路可以知道,D与新制Cu(OH)2加热条件下反应,酸化后得苯乙酸,则D的结构简式为:![]() ;C催化氧化生成D,则C的结构简式为:
;C催化氧化生成D,则C的结构简式为:![]() ;B水解生成C,则B的结构简式为:
;B水解生成C,则B的结构简式为:![]() ;A与溴化氢在双氧水的作用下发生加成反应生成B,所以A为
;A与溴化氢在双氧水的作用下发生加成反应生成B,所以A为![]() ,反应Ⅰ所涉及的物质均为烃,氢的质量分数均相同,比较苯与A的结构可以知道,苯与X发生加成反应生成A,所以X为CH≡CH;苯乙酸与乙醇在浓硫酸作用下发生酯化反应生成E为
,反应Ⅰ所涉及的物质均为烃,氢的质量分数均相同,比较苯与A的结构可以知道,苯与X发生加成反应生成A,所以X为CH≡CH;苯乙酸与乙醇在浓硫酸作用下发生酯化反应生成E为![]() ,E发生取代反应生成F,F与氢气发生加成,醛基转化为羟基,则G的结构简式为:
,E发生取代反应生成F,F与氢气发生加成,醛基转化为羟基,则G的结构简式为:![]() ,G发生消去反应生成H;
,G发生消去反应生成H;
(1)结合以上分析可知,A为![]() ,苯分子中所有原子共平面,乙烯分子中所有原子共平面,所以该有机物分子中最多有6+5+5=16个原子在同一平面上;根据苯乙烯的结构
,苯分子中所有原子共平面,乙烯分子中所有原子共平面,所以该有机物分子中最多有6+5+5=16个原子在同一平面上;根据苯乙烯的结构 可知,苯乙烯分子中最多有3个碳原子在一条直线上;综上所述,本题答案是:16,3。
可知,苯乙烯分子中最多有3个碳原子在一条直线上;综上所述,本题答案是:16,3。
(2)结合以上分析可知,苯与乙炔发生加成反应生成苯乙烯,反应Ⅰ反应类型为加成反应;根据E、F两种物质的结构简式可知,E发生取代反应生成F,反应Ⅱ的反应类型是取代反应;G的结构简式为:![]() ,G发生消去反应生成H,反应Ⅲ的反应类型是消去反应;综上所述,本题答案是:加成反应,取代反应,消去反应。
,G发生消去反应生成H,反应Ⅲ的反应类型是消去反应;综上所述,本题答案是:加成反应,取代反应,消去反应。
(3)结合以上分析可知,B的结构简式是:![]() ;E的结构简式为:
;E的结构简式为:![]() ,其分子式为C10H12O2;根据F的结构简式可知,F中含氧官能团的名称是酯基、醛基;综上所述。本题答案是:
,其分子式为C10H12O2;根据F的结构简式可知,F中含氧官能团的名称是酯基、醛基;综上所述。本题答案是:![]() ,C10H12O2,酯基、醛基。
,C10H12O2,酯基、醛基。


 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】如下图所示A是固体金属单质,燃烧时火焰呈黄色。

(1)写出下列转化的化学方程式。
A→B________________;
B→C___________。
(2)列举下列物质的一种主要用途:
A_____________;
B_________________。
(3)在上述物质转化关系图中的化学反应里,没有元素化合价变化的是______(用“A→B”这样的形式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修5:有机化学基础】丁子香酚可用于配制康乃馨型香精及制作杀虫剂和防腐剂,结构简式如图。

(1)丁子香酚分子式为 。
(2)下列物质在一定条件下能跟丁子香酚反应的是 。
a.NaOH溶液 b.NaHCO3溶液 c.FeCl3溶液 d.Br2的CCl4溶液
(3)符合下述条件的丁子香酚的同分异构体共有____________种,写出其中任意任一种结构简式___________。
① 与NaHCO3溶液反应
② 苯环上只有两个取代基
③ 苯环上的一氯取代物只有两种
(4)丁子香酚的某种同分异构体A可发生如下转化(部分反应条件已略去)。
提示:RCH=CHR′![]() RCHO+R′CHO
RCHO+R′CHO

A→B的化学方程式为_______________________,反应类型为______________________。C中滴加少量溴水振荡,主要现象为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知:
N2(g) + 2O2(g) =2 NO2(g) ΔH = +67.7kJ/mol
2N2H4(g) + 2NO2(g) =3N2(g) + 4H2O (g) ΔH = -1135.7kJ/mol
下列说法正确的是
A. N2H4(g) + O2(g) = N2(g) + 2H2O(g) ΔH = -1068 kJ/mol
B. 铂做电极,以KOH溶液为电解质的肼——空气燃料电池,放电时的负极反应式:N2H4 -4e- + 4OH- = N2 + 4H2O
C. 肼是与氨类似的弱碱,它易溶于水,其电离方程式:N2H4 + H2O![]() N2H5+ + OH-
N2H5+ + OH-
D. 2NO2![]() N2O4,加压时颜色加深,可以用勒夏特列原理解释
N2O4,加压时颜色加深,可以用勒夏特列原理解释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)21世纪是钛的世界,钠米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。工业上二氧化钛的制备是:

I.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4。
II.将SiCl4分离,得到纯净的TiCl4,所采取的操作名称是_______
III.用TiCl4制备TiO2·xH2O的化学方程式为________________,制备时需要________,促进水解趋于完全。
IV.TiO2·xH2O高温分解得到TiO2。如在实验室中进行,则需在________(填仪器名称)中加热。
(2)亚硫酰氯(SOCl2)是一种液态化合物,沸点为77℃,在农药制药等领域用途广泛。SOCl2遇水剧烈反应,液面上有白雾形成,并有带刺激性气味的气体逸出,该气体可使品红溶液褪色。根据上述实验,写出SOCl2与水反应的化学方程式_________________________________________________,AlCl3溶液蒸干灼烧得不到无水AlCl3,而用SOCl2与AlCl3·6H2O混合共热,可得无水AlCl3,其原因是______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空。
(1)按以下实验方案可从海洋物质样品中提取具有抗肿瘤活性的天然产物。

则(1)、(2)、(3)、(4)的分离提纯方法依次为________、________、________、________。
(2)以下分离提纯方法不正确的是______(填字母)
A | B | C | D |
除去硝酸钾中混有的氯化钠 | 从溴单质的四氯化碳 溶液中提取出Br2 | 四氯化碳和水的分离 | 用自来水制取蒸馏水 |
重结晶 | 萃取 | 蒸馏 | 蒸馏 |
(3)下列物质保存方法正确的是______(填字母)
A | B | C | D |
|
|
|
|
(④) | (⑤) | (②⑥) | ( ①③) |
①NaOH溶液 ②浓硫酸 ③Na2CO3溶液 ④白磷 ⑤硝酸银溶液 ⑥酒精
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼、铝、镓、铟、铊是第ⅢA族元素,它们在工农业生产中应用非常广泛。
(1)基态硼原子的核外电子排布图为______________________。
(2)I1(Mg)___________I1(Al)(填“大于”或“小于”),其原因是______________________。
(3)三氯化铝加热到177.8℃时,会升华为气态二聚氯化铝(Al2Cl6,其中铝原子和氯原子均达8电子稳定结构),请写出二聚氯化铝(Al2Ci6)的结构式:______________________,其中铝原子轨道采用___________杂化。
(4)BF4-的空间构型为___________,与BF4-互为等电子体的分子是___________ (写化学式,任写一种即可)。
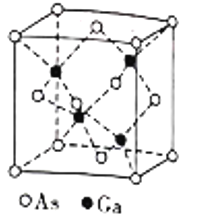
(5)镓(Ga)可与砷(As)形成砷化(GaAs)晶体,该晶体的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________。Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1,阿伏加德罗常数值为NA,则晶胞中Ca与As原子的核间距为___________pm。(列出字母表达式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在环保、化工行业有一种溶液浓度的表示方法:质量—体积浓度,用单位体积溶液中所含的溶质质量来表示,单位g·m-3或g·L-1。现有一种20 ℃时的饱和CuSO4溶液,密度为1.2 g·cm-3,质量—体积浓度为200 g·L-1,则对此溶液的说法不正确的是( )
A. 该溶液的质量分数为16.7%
B. 该溶液的物质的量浓度为1.25 mol·L-1
C. 在20 ℃时,硫酸铜的溶解度为20 g
D. 在20 ℃时把200 g CuSO4·5H2O溶解于1 L水中恰好得到饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大。I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)![]() I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )
I3-(aq)。测得不同温度下该反应的平衡常数如下图所示,下列说法正确的是( )

A. 反应I2(aq)+I-(aq)![]() I3 -(aq)的ΔH>0
I3 -(aq)的ΔH>0
B. 利用该反应可以除去硫粉中少量的碘单质
C. 在上述平衡体系中加入CCl4,平衡不移动
D. 25℃时,在上述平衡体系中加入少量KI固体,平衡常数K小于680
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com