
在一定温度下的密闭容器中,当下列物理量不再变化时,表明A(s)+2B(g)⇌C(g)+D(g)已达平衡的是()
A. 混合气体的压强 B. 混合气体的密度
C. 混合气体的分子数目 D. 混合气体的总物质的量
考点: 化学平衡状态的判断.
专题: 化学平衡专题.
分析: 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答: 解:A、混合气体的压强始终不变,故A错误;
B、混合气体的密度,说明气体的物质的量不变,达平衡状态,故B正确;
C、混合气体的分子数目,始终不变,故C错误;
D、混合气体的总物质的量,始终不变,故D错误;
故选B.
点评: 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案科目:高中化学 来源: 题型:
元素周期表是化学学习和科学研究的重要工具,下列对于元素周期表的使用方法不正确的是( )
|
| A. | 为新元素的发现及预测它们的原子结构和性质提供线索 |
|
| B. | 利用元素周期表发现元素的种类和原子的种类相同 |
|
| C. | 在周期表中金属与非金属的分界处,可寻找半导体材料 |
|
| D. | 指导人们在过渡元素中寻找催化剂和耐高温.耐腐蚀的合金材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知两个热化学方程式:C(s)+O2(g)═CO2(g)△H=﹣393.5kJ/mol2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol.现有炭粉和H2组成的悬浮气共0.3mol,使其在O2中完全燃烧,共放出87.71kJ的热量,则炭粉与H2的物质的量之比是()
A. 1:1 B. 1:2 C. 2:3 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:醋酸是弱酸,其电离过程的△H>0,而强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH﹣(aq)═H2O(l);△H=﹣57.3kI/mol,向1L 0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸;②浓硫酸;③稀硝酸,恰好完全反应时的反应热△H1、△H2、△H3的关系正确的是()
A. △H1>△H2>△H3 B. △H1<△H3<△H2 C. △H1<△H2<△H3 D. △H1>△H3>△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
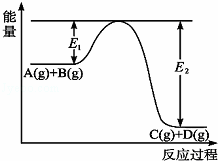
反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
(1)该反应是 (填“吸热”或“放热”)反应.
(2)当反应达到平衡时,升高温度,A的转化率减小(填“增大”“减小”或“不变”),原因是 .
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 ,E2 (填“增大”“减小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,属于水解反应的是()
A. CH3COOH+H2O⇌CH3COO﹣+H3O+ B. CO2+H2O⇌HCO3﹣+H+
C. CO32﹣+H2O⇌HCO3﹣+OH﹣ D. HS﹣+H2O⇌S2﹣+H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的说法正确的是()
A.在测定中和反应的反应热实验中,至少要读两次温度
B.可用pH试纸测定新制氯水的pH
C.中和滴定实验中,洗净后的锥形瓶不需要干燥
D.向CH3COONa溶液中滴入石蕊试液,溶液变蓝
E.向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:C(s)+O2(g)=CO2(g);△H=﹣393.5kJ/mol
H2(g)+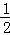 O2(g)=H2O(l);△H=﹣241.8kJ/mol
O2(g)=H2O(l);△H=﹣241.8kJ/mol
欲得到相同的热量,需分别燃烧固体碳和氢气的质量比约为()
A. 2:3.25 B. 12:3.25 C. 1:1 D. 393.5:241
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com